
某兴趣小组的同学在实验室用含有少量氯化钙的氯化钠固体配制一定质量分数的氯化钠溶液,实验步骤如下图所示:
请回答:
(1)在“操作2”中,要用到的玻璃仪器除玻璃棒、烧杯外,还有 。
(2)加入“适量稀HCl”的目的是 。
(3)生成沉淀C的化学方程式 。
(4)“操作3”的名称是 。
(5)用提纯的NaCl配制50g质量分数为 6%的氯化钠溶液,需要NaCl的质量为 g。
(6)如配制50g质量分数为3%的氯化钠溶液所需质量分数为6%的氯化钠溶液(密度为1.04g/cm3)和水的质量分别为:6%的氯化钠溶液体积 mL;水 g。
(7)在用量筒量取所需水的过程中,若俯视读数,而其余操作均正确,这样配得的溶液的溶质质量分数会 (填“偏高”、“偏低”、或“无影响”)。
(1)漏斗; (2)除去溶液中的碳酸钠、氢氧化钠; (3)CaCl2+Na2CO3=2NaCl+CaCO3↓;
(4)蒸发;(5)3; (6)24.04; 25; (7)偏高
解析试题分析:(1)要将不溶性的固体分离,需要进行过滤操作,过滤需要的玻璃仪器有:烧杯、漏斗、玻璃棒;
(2)加入碳酸钠后,和氢氧化钙反应生成了碳酸钙沉淀和氢氧化钠,所以溶液B中存在反应剩余的碳酸钠和生成的氢氧化钠,但是两者对于氯化钠都是杂质,所以加入稀盐酸是为了除去溶液中的氢氧化钠和碳酸钠;
(3)根据稀盐酸和碳酸钙的反应原理书写方程式。碳酸钠和氯化钙反应生成氯化钠和碳酸钙沉淀,方程式是:CaCl2+Na2CO3=2NaCl+CaCO3↓;
(4)氯化钠的溶解度受温度影响变化较小,要得到氯化钠晶体需要蒸发溶剂;
(5)溶质质量=溶液质量×溶质质量分数,是50g×6%=3g;
(6)配制50g质量分数为3%的氯化钠溶液所需质量分数为6%的氯化钠溶液(密度为1.04g/cm3)的质量是: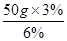 =25g,体积是:
=25g,体积是: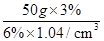 ≈24.04mL,则需要水的质量为50g﹣25g=25g;
≈24.04mL,则需要水的质量为50g﹣25g=25g;
(7)根据正确使用量筒读数的方法进行分析,并进而分析溶质的质量分数变化。在使用量筒读数时,视线要与凹液面的最低处保持水平,俯视导致读数偏大,实际量取液体就偏少,所以导致溶液浓度偏高。
考点:考查一定溶质质量分数的溶液的配制


科目:初中化学 来源: 题型:填空题
为了证明长期暴露在空气中的氢氧化钠溶液已经部分变质,请分别选用两种不同物质类别的试剂完成证明,按要求填写:
(1)选用的试剂为 ,实验现象为 。
(2)选用的试剂为 ,实验现象为 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
从HCl、NaCl、NaOH、Na2CO3、Ca(OH)2几种溶液中取出其中的两种混合,可能的组合共有__________种。
(1)若混合后溶液质量减小,可能的组合是___________________、_________________。
(2)若混合的溶液质量不变,但发生了化学反应,有关的化学方程式为:_________________
_______________、________________________________________。
(3)将稀硫酸逐滴滴入剩下的几种组合种,若产生气体与加入稀硫酸有如图所示的关系,则这样的组合可能是_______________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
下列有三种制取硝酸铜的方案:
方案一:Cu+4HNO3(浓)=Cu(NO3)+2NO2↑+2H2O
方案二:3Cu+8HNO3(稀)=3Cu(NO3)+2NO↑+4H2O
方案三:2Cu+O2+4HNO3(稀)=2Cu(NO3)2+2H2O
请你从经济、环保的角度分析考虑选择一种最适宜的方案 ,你选择方案而不选其它方案的理由是(写两点): ;
.
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
粗盐中含有可溶性杂质(氯化镁、氯化钙等)和不溶性杂质。粗盐提纯的操作步骤如下。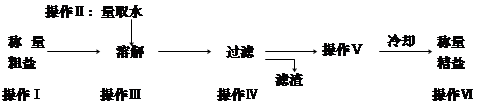
(1)上述过程中除去的杂质是 ;
(2)操作Ⅰ的目的是:a ;b.计算产率;
(3)量取水需要用到的仪器是 ;
(4)操作Ⅴ是 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
在用稀盐酸和氢氧化钠溶液研究中和反应实验时,某化学兴趣小组认真观察、详实记录,进行了一些探究活动.请完成下列问题:
(1)小明同学利用“pH计”测定并绘制了溶液的酸碱度变化如图所示.
①化学方程式为 .
②根据图示可知:小明的实验是用胶头滴管逐滴将 (选填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中至过量.
③在加入溶液的质量至5g时,所得溶液中溶质的化学式为 .
(2)在实验进行几秒钟之后,细心的小华同学发现溶液中有少量气泡冒出.经过小组讨论,他们一致认为NaOH溶液在空气中变质了,依据是 .
为此,他们还进一步设计了两个检验NaOH溶液是否变质的实验方案来重复验证:
方案一:取少量溶液样品,滴入Ca(OH)2溶液,若有白色沉淀生成,则证明NaOH溶液变质了.
方案二:取一定量溶液样品,滴加适量酚酞溶液,若溶液仍为无色,则证明NaOH溶液变质了.
你不同意上述两个实验方案中的哪一个?简述你的理由 .
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
写出将下列物质中所含杂质转化为主要成分的化学方程式(括号内的为杂质):
(1)Na2SO4(H2SO4): ;
(2)Na2CO3(NaOH): ;
(3)NaOH(Na2CO3): ;
(4)CaCl2(CaCO3): ;
(5)NaCl(BaCl2): 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
某研究性学习小组设计了测定纯碱样品(含NaCl杂质)中碳酸钠质量分数的实验方案。请回答下列问题:
(1)碳酸根离子沉淀法。实验步骤:
①用托盘天平称取wg样品放入烧杯中加水溶解;
②加入足量的BaCl2溶液成分反应,证明反应后剩余的方法是_______________________________________;
③过滤、洗涤、称量沉淀的质量为mg;④样品中碳酸钠的质量分数为_______________________。
(2)气体法。学习小组利用右图装置测定样品中碳酸钠的质量分数。
①实验装置乙中盛放的试剂为______________,装置丁的作用是______________________________________
______________________。
②学习小组通过测量丙装置实验前后的质量,确定二氧化碳的质量。实验中滴加稀硫酸的速度过快,产生的气流过急,会导致测得样品中碳酸钠的质量分数______________(填写“偏高”、“偏低”或“不变”)。
(3)测氯化钠法。请你完成下列实验方案:称取一定质量的样品放入烧杯中加水溶解;____________________
________________________________________________________________________________________;过滤、洗涤、干燥称量沉淀的质量。计算出氯化钠的质量,再得样品中碳酸钠的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com