
小强去商店买回一包纯碱,包装说明如右图.为测定该纯碱中碳酸钠含量是否符合标签要求,他称取了纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g.试求:
(1)反应放出的CO2的质量为 g。
(2)纯碱样品中碳酸钠的质量。
(3)根据这一次检测,计算并判断样品中碳酸钠的含量是否符合标签要求。
(1)4.4g (2)10.6g (3)不符合标签要求。
解析试题分析:(1)根据质量守恒定律可以求算出生成的二氧化碳的质量;
(2)根据二氧化碳的质量结合化学方程式可以求算出碳酸钠的质量,根据质量分数的计算公式计算出碳酸钠的质量;
(3)根据(2)碳酸钠的质量即可求出碳酸钠的质量分数后与包装说明相比较即可完成解答。
解:(1)根据质量守恒定律可以知道生成二氧化碳的质量为:11g+50g+64.4g﹣121g=4.4g;
(2)设纯碱样品中碳酸钠的质量为x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g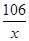 =
=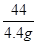
解得:x=10.6g
(3)纯碱样品中碳酸钠的质量分数为: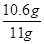 ×100%=96.4%
×100%=96.4%
因为96.4%<98%,所以该纯碱样品中碳酸钠的质量分数不符合标签要求。
答:(2)纯碱样品中碳酸钠的质量为10.6g;
(3)该纯碱样品中碳酸钠的质量分数不符合标签要求。
考点:考查根据化学反应方程式的计算


科目:初中化学 来源: 题型:单选题
某化学实验小组要检测黄铜(铜、锌合金)中金属铜的纯度,同学们取20g黄铜样品,向其中分三次共加入15g盐酸溶液,充分反应后测得实验结果如下:
| 实验次数 | 1 | 2 | 3 |
| 盐酸质量 | 5g | 5g | 5g |
| 氢气质量 | 0.04g | m | 0.02g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
人体缺乏维生素C(简写Vc)会患坏血病。下图所示为某种“维生素C”说明书的一部分,请回答:
(1)Vc中C、H、O三种元素的质量比是 。
(2)若正常成人每天对Vc的最低需要量为60mg。
①当这些Vc完全来自右图的“维生素C”时,则每次服用“维生素C”至少 片;
②当这些Vc完全来自某种新鲜蔬菜(每1000g这种蔬菜含Vc120mg)时,每天至少应食用这种蔬菜 g。
③维生素C又名抗坏血酸,其水溶液能使紫色石蕊试液变 色。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
我国青海湖采集的天然碱样品可表示为aNa2CO3·bNaHCO3·cH2O(a、b、c为最简整数比)。小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验: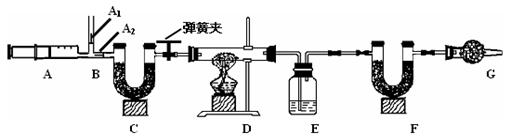
已知:1.碳酸钠比较稳定,加热时不分解 ;2. 2NaHCO3 Na2CO3 +CO2 ↑ +H2O
Na2CO3 +CO2 ↑ +H2O
3.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭。
实验步骤
实验时,组装好装置,实验前应先 ,然后,实验步骤是:
① 反复推拉注射器 ② 称量E、F的质量 ③ 关闭弹簧夹,加热D处试管直到反
应不再进行 ④ 打开弹簧夹,再次反复缓缓推拉注射器 ⑤ 再次称量E、F的质量。
(二)问题探究:
(2) E中的药品为 ,E的作用是 。C、F、G中装有碱石灰(生石灰与烧碱的固体混合物),则C的作用是 , F的作用是 。写出 F装置中所发生反应的一个化学方程式 。
(3)实验步骤②与③能否颠倒 (填“能”或“不能”)。若不进行步骤④的操作,则所测得的碳酸氢钠质量 (填“偏大”、“偏小”、“无影响”), 该操作中推注射器时缓缓的目的是 ;若没有G装置,则碳酸氢钠的质量 (填“偏大”、“偏小”、“无影响”)。
(4)下表是实验记录数据:
| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为102.25g |
| F的质量为50.0g | F的质量为51.1g |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
向20g赤铁矿样品中(样品中杂质不溶于水,也不和酸反应)不断加入稀盐酸至固体量不再减少为止,共消耗稀盐酸184g,测得剩余固体的质量为4g。请计算:
(1)赤铁矿样品中,氧化铁的质量分数
(2)最后所得溶液中溶质的质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(5分)鸡蛋壳的主要成分是碳酸钙.小明同学为了测定鸡蛋壳中碳酸钙的质量分数,分别设计了如下实验并进行计算.将鸡蛋壳洗净、干燥并捣碎后放入锥形瓶里,加入足量的稀盐酸充分反应(假设其他杂质不与盐酸反应).
测得相关数据如图所示:
【数据处理】
(1)反应生成二氧化碳的质量为 g.
(2)请帮小明计算鸡蛋壳中碳酸钙的质量分数,并写出计算过程:
实验过程如果有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比 (填“偏大”、“偏小”或“不变”)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(5分)哈南新城在地铁建设中需要大量的钢铁,现有赤铁矿样品(所含杂质不溶于水也不与酸反应),实验小组同学为测定其纯度,
进行了三次实验,实验数据如下表所示。请回答下列问题:
| | 第1次 | 第2次 | 第3次 |
| 样品质量(g) | 25 | 30 | 25 |
| 盐酸质量(g) | 200 | 100 | 100 |
| 所得溶液质量(g) | 216 | 116 | 116 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
实验室有一瓶硫酸废液,老师请小红同学设计方案测定该废液中硫酸的质量分数.小红同学先取一纯净小烧杯,称其质量为18.2g,然后往其中倒入少量硫酸废液后称量,总质量为33.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸砂去铁锈)放入该小烧杯中反应,待铁钉表面不再有气泡产生后,再次称量,总质量为43.9g.请回答下列问题:
(1)反应中产生的气体的质量是 。
(2)计算该废液中硫酸的质量分数(写出计算过程,计算结果保留一位小数).
(3)如果铁钉的铁锈未除净,对(2)计算结果的影响是 (选填“偏大”、“偏小”、“无影响”),原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
(3分)过氧化钙(CaO2)与水反应可产生氧气:2CaO2+2H2O=2Ca(OH)2+O2↑,因此广泛用于水产养殖、污水处理等领域。若用288 g过氧化钙来给鱼池增氧,理论上可释放出多少克氧气?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com