
| A. | 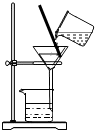 分离氢氧化钡溶液和盐酸反应后的生成物 | |
| B. | 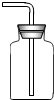 收集CO2气体 | |
| C. | 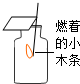 检验二氧化碳是否收集满 | |
| D. |  确认CO2和NaOH已发生反应 |
分析 A、氢氧化钡溶液和盐酸反应后生成物是氯化钡和水,氯化钡易溶于水,据此进行分析判断.
B、根据二氧化碳的收集方法进行分析判断.
C、根据二氧化碳气体的验满方法进行分析判断.
D、根据二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,会造成装置内压强减小;滴加稀盐酸,碳酸钠溶液能与稀盐酸反应生成氯化钠、水和二氧化碳,会造成装置内压强增大,据此进行分析判断.
解答 解:A、氢氧化钡溶液和盐酸反应后生成物是氯化钡和水,氯化钡易溶于水,不能用过滤的方法进行分离,故选项装置或操作不能达到实验目的.
B、二氧化碳密度比空气的大,应用向上排空气法收集,但集气瓶口不能塞塞子,否则空气无法排出,故选项装置或操作不能达到实验目的.
C、检验二氧化碳是否收集满时,应将燃着的木条放在集气瓶口,不能伸入瓶中,故选项装置或操作不能达到实验目的.
D、二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,会造成装置内压强减小,会观察到气球变大;滴加稀盐酸,碳酸钠溶液能与稀盐酸反应生成氯化钠、水和二氧化碳,会造成装置内压强增大,会观察到气球变小,恢复原状;根据气球的变化,可确定CO2和NaOH已发生反应,故选项装置或操作能达到实验目的.
故选:D.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
 现有A、B、C、D、E、F、G七种物质,C、F是常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图所示转化关系,回答下列问题:
现有A、B、C、D、E、F、G七种物质,C、F是常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图所示转化关系,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| KNO3 | Ca(NO3)2 | Na(NO3)2 | Mg(NO3)2 | Al(NO3)3 | Zn(NO3)2 | Fe(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂质的试剂和方法 | |
| A | NaOH | Na2CO3 | 加入适量的稀盐酸,蒸发 |
| B | CaO | CaCO3 | 高温煅烧后冷却 |
| C | FeCl2 | CuCl2 | 溶解,过滤,蒸发 |
| D | Zn | Cu | 加入足量稀盐酸后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③⑤ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 莽草酸中氢元素的质量分数最大 | B. | 莽草酸由碳、氢、氧三种元素组成 | ||
| C. | 莽草酸中各元素的质量比为7:10:5 | D. | 每个莽草酸分子里含有5个氢分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com