
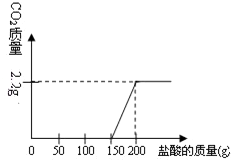
 某中学实验室一小瓶氢氧化钠变质后质量为18.3g(假设只有氢氧化钠、碳酸钠和水三种物质),现将其配成102.2g溶液,向其中滴入稀盐酸.滴加过程中产生的二氧化碳的质量与加入的稀盐酸的质量之间的关系如图所示.试计算:
某中学实验室一小瓶氢氧化钠变质后质量为18.3g(假设只有氢氧化钠、碳酸钠和水三种物质),现将其配成102.2g溶液,向其中滴入稀盐酸.滴加过程中产生的二氧化碳的质量与加入的稀盐酸的质量之间的关系如图所示.试计算:| 73 |
| x |
| 117 |
| y |
| 44 |
| 2.2g |
| 40 |
| z |
| 58.5 |
| a |
| 36.5 |
| 10.95g |
| 23.4g |
| 102.2g+200g-2.2g |


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:初中化学 来源: 题型:
 实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题:
实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
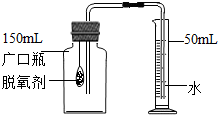 (2011?南平)食品安全,关乎民生.食品脱氧剂(以活性铁粉为主的物质组成)能通过化学反应除去密闭包装袋中的氧气,使食品处于无氧状态,有效控制细菌、霉菌的生长,以保持食品的色、香、味.
(2011?南平)食品安全,关乎民生.食品脱氧剂(以活性铁粉为主的物质组成)能通过化学反应除去密闭包装袋中的氧气,使食品处于无氧状态,有效控制细菌、霉菌的生长,以保持食品的色、香、味.| 实验所需的时间/min | 0 | 5 | 10 | 30 | 35 | 45 |
| 量筒中液面的刻度/ml | 50 | 35 | 27.5 | 20 | 20 | 20 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题:
实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题:查看答案和解析>>
科目:初中化学 来源:2010年黑龙江省哈尔滨市中考化学模拟试卷(一)(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com