
| A. | 发生反应的甲和乙的质量比为22:3 | B. | 生成物丙和丁均为氧化物 | ||
| C. | 生成的丙和丁的分子个数比为1:1 | D. | 反应前后原子总数不变 |
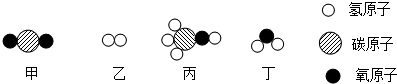
分析 根据微观示意图分析反应物、生成物的化学式,根据反应写出反应的化学方程式.根据化学式、方程式的意义计算、分析、判断有关的问题.
解答 解:由反应的微观示意图可知,该反应是二氧化碳和氢气在一定条件下反应生成了甲醇和水,反应的方程式是:CO2+3H2$\frac{\underline{\;一定条件\;}}{\;}$CH3OH+H2O.
A、由反应的方程式可知,发生反应的甲和乙的质量比为44:(3×1×2)=22:3,故结论正确;
B、由反应的方程式可知,生成物丙为CH3OH,有三种元素成,不属于氧化物,丁均为H2O,属于氧化物.故结论不正确;
C、由上述方程式可知,生成的丙和丁的分子个数比为1:1,故结论正确;
D、由微粒的变化可知,反应前后原子总数不变,故D正确.
故选项为:B.
点评 本题属于微观示意图的考查,解答本题比较简便的方法是根据微观示意图写出反应的化学方程式,根据方程式的意义分析解答.


 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:初中化学 来源: 题型:实验探究题
| 离子 | OH- | Cl- | SO42- |
| H+ | 溶、挥 | 溶 | |
| Na+ | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 |
| Cu2+ | 不 | 溶 | 溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
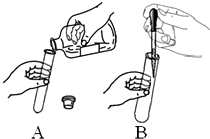 如图中是某同学验证中和反应的实验操作.A是取用稀盐酸的操作,B是向稀盐酸和酚酞的混合液中滴加NaOH溶液的示意图.
如图中是某同学验证中和反应的实验操作.A是取用稀盐酸的操作,B是向稀盐酸和酚酞的混合液中滴加NaOH溶液的示意图.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 泥水中,泥是溶质,水是溶剂 | |
| B. | 物质的溶解过程通常会伴随着能量的变化 | |
| C. | 配制溶液时,搅拌可以增大固体物质的溶解度 | |
| D. | 15℃时硝酸钾的溶解度为25g,则该温度下硝酸钾饱和溶液中溶质与溶剂的质量比为1:5 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 实验步骤 | 实验现象 | |
| 实验1 | 取样与试管中,加入食醋 并将产生气体通入澄清石灰水中 | 有气泡产生 石灰水变浑浊 |
| 实验2 | 取安多夫样品少许加入试管中,加热使之充分反应,并把产生的气体通入澄清石灰水 | 试管口出现小水珠,澄清石灰水变浑浊,试管中残留白色固体粉末 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 这里的“高钙”是指钙元素 | B. | 蛋白质、糖类都能为人体提供能量 | ||
| C. | 糖类由C、H、O三种元素组成 | D. | 人体缺钙易引起甲状腺肿大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com