
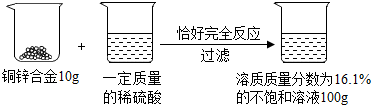
分析 根据铜不能和稀硫酸反应,锌能和稀硫酸反应生成硫酸锌和氢气,最后所得溶液是硫酸锌溶液,根据硫酸锌溶液的质量、溶质质量分数可以计算反应生成氢气的质量、锌的质量、硫酸的质量,进一步可以计算合金中铜的质量分数和所用稀硫酸的溶质质量分数,溶液稀释前后,溶质质量不变进行分析.
解答 解:(1)根据图示知,最终生成的不饱和溶液中溶质的质量为16.1g;
(2)设锌的质量为y,参加反应的硫酸的质量为z,
Zn+H2SO4═ZnSO4 +H2↑,
65 98 161
y z 100g×16.1%
$\frac{65}{y}$=$\frac{98}{z}$=$\frac{161}{100g×16.1%}$,
y=6.5g,z=9.8g,
合金中铜的质量分数为:$\frac{10g-6.5g}{10g}$×100%=35%;
(3)设稀硫酸的质量为m,
6.5g+m-0.2g=100g
m=93.7g,
所用稀硫酸的溶质质量分数为:$\frac{9.8g}{93.7g}$×100%=10.5%
答:所用稀硫酸的溶质质量分数为10.5%;
(4)设在配制过程中需要另外加水为n,
需要浓硫酸的质量为:$\frac{9.8g}{98%}$=10g,
所以n=93.7g-10g=83.7g.
故答案为:(1)16.1g;
(2)35%;
(3)10.5%;
(4)83.7g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 物 质 | 所选试剂和操作 |
| A | BaSO4(BaCO3) | 加足量稀盐酸、过滤、洗涤、干燥 |
| B | KCl(K2CO3) | 加足量稀硫酸、过滤、蒸发、结晶 |
| C | CuO(Cu) | 在空气中充分灼烧 |
| D | CO(HCl气体) | 足量的NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 浓硫酸具有吸水性,所以浓盐酸也具有吸水性 | |
| B. | 酸雨的pH小于7,所以pH小于7的雨水一定是酸雨 | |
| C. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| D. | 组成CO和CO2的元素相同,但它们的分子构成不同,所以它们的化学性质不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
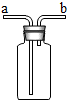 如图所示装置(不可倒置)有多种用途,下列叙述正确的是C
如图所示装置(不可倒置)有多种用途,下列叙述正确的是C查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com