
【题目】下图是A、B、C三种固体物质的溶解度曲线。

(1)溶解度随温度升高而明显增大的物质是_________。
(2)t1℃时,三种物质溶解度的大小关系是_________。
(3)A中含有少量C,提纯A采用的方法是_________。
(4)t2℃时,A和B各40g分别加入100g水中,充分搅拌,不能形成饱和溶液的是______。要使该不饱和溶液变为饱和溶液,除了增加溶质,还可以采用的一种方法是______。
 口算能手系列答案
口算能手系列答案科目:初中化学 来源: 题型:
【题目】某粗盐样品中含有杂质氯化镁、氯化钙。康康设计了以下提纯方案:
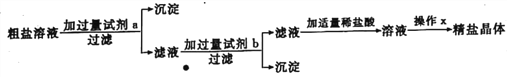
(1)过滤和操作x中都用到的玻璃仪器是____________,其在操作x中的作用是__________。
(2)加入试剂b后,必须过滤,否则滴加稀盐酸后沉淀会溶解,沉淀溶解的化学方程式为_________________。(只写1个)。
(3)滴加稀盐酸时产生气体的情况如图所示,OA段发生反应的化学方程式为_____________________。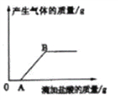
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列反应的化学方程式,并按要求填空。
(1)工业上用一氧化碳和赤铁矿(主要成分是三氧化二铁)在高温下炼铁:__________。
(2)生石灰作为干燥剂: ____________________,该反应属于_________ (选填“放或吸热”)。
(3)用氢氧化钠溶液吸收少量二氧化硫气体:___________________________________。
(4)用稀硫酸除去铁锈:_____________________,反应后所得溶液的颜色为_________色。
(5)硫酸铵固体和氢氧化钙固体混合研磨:___________,该反应的基本反应类型是_______。
(6)生成沉淀的中和反应:_________________________________,恰好完全反应后液体的导电性比反应前的______ (选填“增强”、“减弱”或“不变”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组的甲、乙两同学围绕Na2CO3进行了如图一所示的实验.实验结束后,丙同学把A、B两支试管中的物质倒入同一洁净的烧杯中(如图二),充分混合后发现白色沉淀明显增加,结合题目信息,回答以下问题:
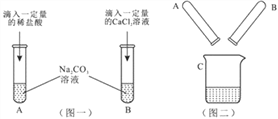
(1)甲同学的实验完成后,A试管一定有剩余的物质是_________。
(2)B试管的实验发生的化学方程式是________________。
小组同学将C中液体过滤后,对所得滤液的主要成分进行了如下探究:
【猜想与假设】实验小组的同学对滤液的成分作出了如下猜想:
猜想一:滤液中的溶质是NaCl、Na2CO3
猜想二:滤液中的溶质是_______。。
猜想三:滤液中的溶质是NaCl、CaCl2、Na2CO3
猜想四:滤液中的溶质是NaCl
【讨论与交流】通过认真讨论,小组同学排除了其中一种不合理的猜想。
(3)你认为不合理的猜想是_______,理由是______。
【进行实验】丁同学取少量滤液置于试管中,向试管中滴加一种物质,发现有无色气泡生成。
(4)你认为丁同学向滤液中滴加的物质是_________。
【实验结论】通过探究,小组同学得出了猜想一成立的结论。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将含有少量Na2SO4的NaCl样品10 g溶于80 g水,再向其中滴加70 g BaCl2溶液,恰好完全反应,过滤后称得滤液的质量为157.67 g,求样品中NaCl的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】创建“水美城市”,亮出闽北名片。
(1)八闽首府建州(今建瓯),历史悠久。建瓯板鸭富含的营养素是_______。
(2)百合是南平市花。走在王台百合园区,会闻到幽幽花香。请用微粒的观点解释这一现象:_______。
(3)优质水源是酿酒条件之一,政和“东平老窖”是福建名酒。.酒精(C2H6O)属于_______。(填选项)
A.氧化物 B.碱 C.盐 D.有机物
(4)闽北各地加强环境治理,大力推广沼气池建设。沼气主要成分是甲烷(CH4),甲烷完全燃烧的化学方程式是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】厉害了,我的国,我国大飞机C919首飞成功,新型材料也得到广泛应用。中华儿女正在民族复兴的道路上“撸起袖子加油干!”

(1)用来制造无人机的铝合金属于______(填“纯净物”或“混合物”)。自然界中存在碳-12、碳-13、碳-14三种不同的原子,这三种原子都属于同种元素的原因是 _______________。
(2)某种无人机的动力来源于锂电池,锂电池的工作原理是FePO4+Li![]() LiFePO4,则锂电池放电时的反应类型是______反应;在LiFePO4中锂元素显+1价,磷元素显+5价.则铁元素的化合价是______。
LiFePO4,则锂电池放电时的反应类型是______反应;在LiFePO4中锂元素显+1价,磷元素显+5价.则铁元素的化合价是______。
(3)大飞机C919发动机上的压气机将高密度空气(高压压缩后的空气)压入燃烧室,能促进航空煤油燃烧,使燃油消耗减少16%。请你从微观角度解释高密度空气能使航空煤油燃烧更充分的原因是_______________________,应用该技术的重要意义是__________________(作答一点)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钢铁行业是我国国民经济的支柱性产业,我国钢铁生产总量占世界钢铁生产总量的50%以上。
⑴钢是一种铁合金,其硬度比纯铁________(填“大”或“小”),钢铁生锈实际是铁与空气中的________发生了化学反应。请写出一种能防止钢铁生锈的措施______________。
⑵下图是某兴趣小组用实验室装置模拟炼铁的化学原理图,用于测定赤铁矿中氧化铁的质量分数。
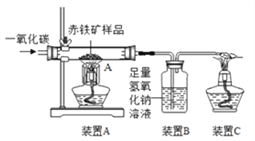
①装置A中发生反应的化学方程式为___________;装置B中发生反应的化学方程式为________;装置C的作用是______________;
②装置气密性良好,假设反应完全且赤铁矿中的杂质不参加反应,称重赤铁矿样品的质量为wg,则要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是____________或_____________。
⑶某研究性学习小组将Fe和Fe2O3的混合物与稀硫酸反应以测定混合物中Fe2O3的质量分数。称取样品27.2g,与质量分数为20%的稀硫酸充分反应,当加入196g稀硫酸时固体粉末恰好完全溶解,此时收集到0.2g氢气,请写出Fe和Fe2O3分别与稀硫酸反应的化学方程式__________、_________。
【提出疑问】小明根据已有知识推断固体溶解后溶液中的溶质为Fe2(SO4)3和________,并据此计算出铁的质量5.6g,进一步计算发现需要硫酸的总质量比实际消耗的________(填“多”或“少”)。
【查阅资料】Ⅰ、含Fe3+的溶液中滴加硫氰化钾(KSCN)溶液后溶液呈红色;含Fe2+的溶液中滴加硫氰化钾溶液后溶液无明显现象。
Ⅱ、Fe2(SO4)3+Fe= 3FeSO4
【继续探究】小明向反应后的溶液中滴加KSCN溶液,无明显现象。则溶液中肯定不含________。
【分析计算】计算出27.2gFe和Fe2O3的混合物中Fe2O3的质量分数______。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生活、生产中有着非常广泛的应用。请回答下列问题:
(1)2017年8月21日,“复兴号”中国标准动车组开跑京津城际,车体是铝合金制成,铝合金是_____ (填字母编号)。
A.有机合成材料 B.金属材料 C.复合材料
(2)十八世纪,化学家们研究发现某些金属与某些物质反应能生成一种气体,该气体被喻为“会制造水的物质”,对上述反应原理的认识加快了推翻燃素学说的进程。该气体在空气中燃烧制造水的化学方程式是_____。
(3)金属R不在初中学到的金属活动性顺序表中,已知R的活动性位于铜、铝之间,某同学为了验证这三种金属的活动性顺序,他选择了打磨过的金属R,你认为他还需要选择的另外两种溶液是_____溶液和________溶液。
(4)工业上常用铝土矿炼制铝,其主要成分为氧化铝,现用200t含氧化铝51%的铝土矿(其他成分不含铝)炼铝,假设在炼制过程中铝元素共计损失了10%,则反应后可制得铝_____t。
(5)铜与另一种金属M的混合物(M可能是铝、铁或银),在该混合物中加入足量的稀硫酸有气泡产生,待反应完成后过滤,得到铜和滤液,在滤液中加入锌片,其表面有一层黑色物质,则M是_____;取一定量的原混合物投入到一定量的硝酸银溶液中,充分反应后,对反应所得溶液和固体推断正确的是_____ (填字母编号)。
A.所得溶液中一定有M的离子 B.固体中一定有银和铜
C.固体中一定有银 D.所得溶液中一定有硝酸银
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com