
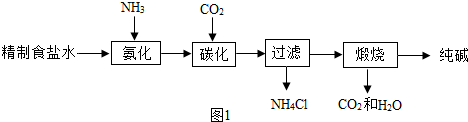

分析 (1)①根据石灰石的主要成分是碳酸钙,在高温下分解生成氧化钙和二氧化碳气体,写出反应的方程式;
②根据浓盐酸具有挥发性,二氧化碳能够和碱性物质反应分析;
(2)①根据常见的化学肥料的特征分析;根据信息写出反应的方程式;根据碳酸氢钠的俗名及用途回答;
②根据过滤的注意事项分析判断;
(3)方案一,根据沉淀的质量计算碳酸钠的质量,从而计算碳酸钠的质量分数,判断产品的等级;
方案二:根据二氧化碳的性质及装置的特点等分析误差.
解答 解:(1)①石灰石的主要成分是碳酸钙,在高温下分解生成氧化钙和二氧化碳气体,故方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
②浓盐酸具有挥发性,会使制得的二氧化碳中混有氯化氢杂质,因此不用浓盐酸;二氧化碳能够和氢氧化钠和氧化钙反应,因此不能被氢氧化钠固体和生石灰干燥;故答案为:浓盐酸具有挥发性,会使制得的二氧化碳中混有氯化氢杂质;A;
(2)①农作物生长需大量的N、P、K元素,含有N元素的肥料属于氮肥;所以NH4Cl可用作氮肥;NH4Cl与Ca(OH)2在加热时发生反应生成产品CaCl2,同时还有NH3和H2O生成,因此反应的方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;碳酸氢钠俗名小苏打,常用于做发酵粉或治疗胃酸过多等;
故答案为:氮;2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;小苏打;做发酵粉或治疗胃酸过多等;
②A.使用的漏斗不是长颈漏斗,故错误;
B.液面应低于滤纸边缘,否则液体得不到过滤,会使滤液浑浊,故正确;
C.玻璃棒起到引流作用,不能搅拌,故错误;
D.漏斗下端的管口要紧靠烧杯内壁,防止液体溅出,故正确;
故答案为:BD;
(3)方案一:解:设产生19.7g碳酸钡沉淀需要碳酸钠的质量为 x
Na2CO3+BaCl2═BaCO3↓+2NaCl
106 197
x 19.7g
$\frac{106}{x}$=$\frac{197}{19.7g}$
解之得:x=10.6g
所以样品中Na2CO3质量分数为:$\frac{10.6g}{10.65g}$×100%=99.5%>99.2%,因此属于优等品;
方案二:A是锥形瓶,本装置通过收集二氧化碳的体积计算碳酸钠及质量分数,但由于二氧化碳能够溶于水且能够和水,会导致收集的二氧化碳偏少,也可能导管中存留一部分水产生误差;
故答案为:锥形瓶;二氧化碳能溶于水且能与水反应,使会导致收集的二氧化碳偏少或导管中存留一部分水产生误差.
点评 本题考查的知识点较多,考查的问题也比较细,能加深学生对课本知识的理解,训练学生的思维能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 汞 水银 Hg 化合物 | |
| B. | 碳酸氢钠 苏打 NaHCO3 盐 | |
| C. | 过氧化氢 双氧水 H2O2 氧化物 | |
| D. | 固态二氧化碳 干冰 CO2 有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 麻黄碱的相对分子质量为165 | |
| B. | 麻黄碱中含有10个碳原子 | |
| C. | 麻黄碱中氢元素的质量分数最大 | |
| D. | 麻黄碱中氮元素与氧元素的质量比1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质甲 | 物质乙 | 物质丙 |
| A | HCl | Zn | AgCl |
| B | H2SO4 | Fe2O3 | NaCl |
| C | Ba(OH)2 | Na2CO3 | CaCl2 |
| D | H2SO4 | Ba(OH)2 | NaCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
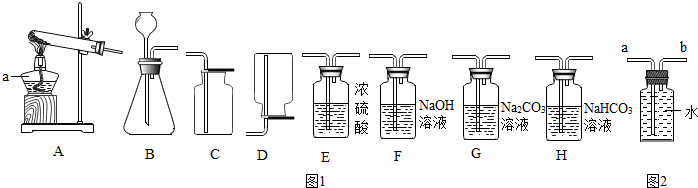
| 实验步骤 | 实验现象 | 实验结论 |
| 气体中有HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com