
【题目】某废水中含有AgNO3、Ca(NO3)2、Fe(NO3)2、Cu(NO3)2、NaNO3几种物质。为了回收金属,同时得到较纯的硝酸钠,保护环境,化学小组的同学设计了一个处理该废水的实验方案,流程如下:

[查阅资料]白色的Fe(OH)2沉淀在潮湿空气中会迅速转化为红褐色的Fe(OH)3。
(1)操作X的名称是_______。
(2)操作中加入过量金属Fe,用铁粉末比铁片更好,其原因是_____,加入过量金属Fe可以除去废水中的______。
(3)溶液C中含有的阴离子有______。
(4)写出白色的Fe(OH)2沉淀转化为红褐色Fe(OH)3反应的化学方程式:______。
(5)化学兴趣小组对以上流程得到的NaNO3液进行检测,分析后可知得到的NaNO3溶液不纯,含有杂质,则最后得到的NaNO3溶液所含的杂质是_____。
【答案】过滤 增大反应物接触面积,充分反应 AgNO3、Cu(NO3)2 NO3-、OH- 4Fe(OH)2+O2+2H2O=4Fe(OH)3 Na2CO3、NaOH
【解析】
(1)操作X将混合物分离得到固体和溶液,所以操作X是过滤。
故填:过滤。
(2)铁粉优点是增大反应物间的接触面积,使反应更快、更充分,铁的活动性较银和铜强,可将银和铜从它们的化合物溶液中置换出来,所以加入过量的铁粉可除去硝酸银和硝酸铜。
故填:增大反应物接触面积,充分反应;AgNO3、Cu(NO3)2。
(3)溶液B中的溶质是硝酸亚铁、硝酸钠和硝酸钙,加入过量的氢氧化钠后,硝酸亚铁转化为氢氧化亚铁,所以溶液C中含有的溶质是硝酸钠、硝酸钙、氢氧化钠,对应的阴离子是硝酸根离子和氢氧根离子。故填:NO3-、OH-。
(4)氢氧化亚铁在空气中转化为氢氧化铁,反应物中一定有氢氧化亚铁,生成物是氢氧化铁,分析可知,该反应的反应物为氢氧化亚铁、水和氧气,生成物为氢氧化铁,反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3。
故填:4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(5)由于加入的氢氧化钠和碳酸钠均过量,后续操作中对过量的氢氧化钠和碳酸钠未进行处理,所以最终所得硝酸钠溶液中还有碳酸钠和氢氧化钠。
故填:Na2CO3、NaOH。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】回答下列与金属有关的问题。
(1)黄铜片与铜片互相刻划目的是_____;
(2)铝比铁活泼,但抗腐蚀性能却更强,用化学方程式解释其原因_____;
(3)工业上,把赤铁矿冶炼成铁的主要反应原理是3CO+Fe2O3![]() 2Fe+3CO2,其中_____发生了氧化反应。
2Fe+3CO2,其中_____发生了氧化反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】做完加热铜片的实验后,小明同学对其成分进行分析。取10g此样品,向其中分五次加入相同溶质质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量及剩余固体的质量记录于下表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
充分反应后剩余固体的质量/g | 9.2 | 8.4 | 7.6 | 7 | 7 |
试回答下列问题:
(1)10g样品中氧化铜的质量为__________g。
(2)计算所加入稀硫酸中溶质的质量分数____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中不正确的是( )
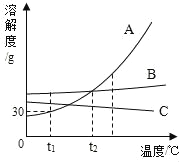
A. t1℃时,A的饱和溶液65g中含有溶剂50g
B. 将t2℃A、B、C三种物质的饱和溶液降温至t1℃时,C溶液中溶质的质量分数保持不变
C. 在t2℃时,A、B两种溶液中溶质的质量分数相同
D. 接近饱和的A溶液中含有少量的杂质B,通常可采用降温结晶的方法来提纯A
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图像不能正确反映对应变化关系的是
A.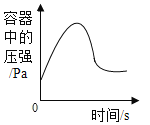 在密闭容器中用红磷测定空气中氧气的含量
在密闭容器中用红磷测定空气中氧气的含量
B.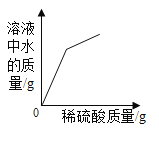 向一定量的氧化铜粉末中逐滴加入稀硫酸至过量
向一定量的氧化铜粉末中逐滴加入稀硫酸至过量
C.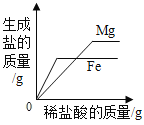 向等质量的镁粉和铁粉中分别加入同浓度的稀盐酸至过量
向等质量的镁粉和铁粉中分别加入同浓度的稀盐酸至过量
D.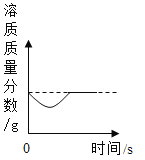 在饱和石灰水中加入少量生石灰
在饱和石灰水中加入少量生石灰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某课外兴趣小组为探究一久置的铝片中铝元素的质量分数,他们取8g该铝片样品放入烧杯中,并依次加入一定质量的相同浓度的稀盐酸,测得相关数据如下,请回答问题。
实验次数 | 1 | 2 | 3 | 4 | 5 |
每次加入稀盐酸的质量/g | 50.0 | 100.0 | 100.0 | 100.0 | 100.0 |
产生气体的总质量/g | 0 | 0.2 | a | 0.6 | 0.7 |
(1)a的数值为_______。
(2)计算所用稀盐酸的溶质质量分数______ (结果保留至0.1%,下同) 。
(3)求该铝片中铝元素的质量分数______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
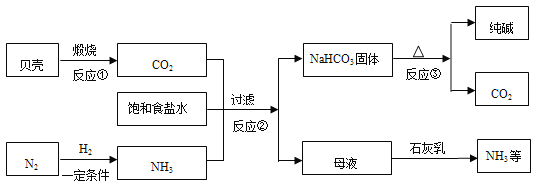
已知:贝壳的主要成分是CaCO3,反应②的化学方程式为:NaCl(饱和溶液)+NH3+H2O+CO2=NH4Cl+NaHCO3↓
(1)反应①的另一种产物是配制石灰乳的主要原料之一,配制石灰乳时发生反应的化学方程式为_____________。
(2)反应③的基本反应类型是_______,反应的化学方程式为________________。
(3)母液中含有的溶质是________。
(4)整个生产过程中可循环利用的物质是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下面的实验过程和提供的数据,回答下列问题。(不考虑反应中水分的蒸发,假设生成的气体全部逸出)
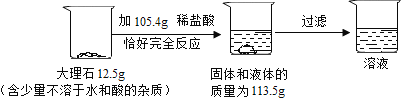
(1)生成的二氧化碳的质量_____g。
(2)过滤后所得溶液中溶质CaCl2 的质量分数_____(精确至0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com