
| 溶质的质量 |
| 溶液的质量 |
| 溶质的质量 |
| 溶液的质量 |
| 78 |
| 109.5 |
| 0.79g |
| 0.39g |


科目:初中化学 来源: 题型:
| A、碳酸氢铵(NH4HCO3) |
| B、硫酸钾 (K2 SO4) |
| C、磷酸二氢铵( NH4H2PO4) |
| D、尿素(CO(NH2)2) |
查看答案和解析>>
科目:初中化学 来源: 题型:
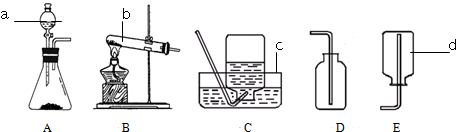
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
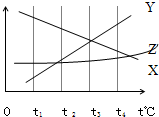 图是X、Y、Z三种物质的溶解度曲线,根据图示回答下列问题:
图是X、Y、Z三种物质的溶解度曲线,根据图示回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 做菜用的一种嫩肉粉其主要成分是碳酸氢钠,可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋(含醋酸)等调料烧煮时会产生大量气泡.他对此颇感兴趣,决定对其进行探究.
做菜用的一种嫩肉粉其主要成分是碳酸氢钠,可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋(含醋酸)等调料烧煮时会产生大量气泡.他对此颇感兴趣,决定对其进行探究.| 实验步骤 | 实验现象 | 实验结论 | |
| 实验1 | 取碳酸氢钠样品少许加入试管中,加热到不产生气体为止,并把产生的气体通入澄清石灰水 | 试管口有小水滴产生 澄清石灰水变浑浊 |
猜想①正确 |
| 实验2 | 猜想②正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验探究 | 实验现象 | 实验结论 |
| ①取少量该溶液于试管中,向其中滴加过量的氯化钡溶液 | 生成白色沉淀 | 假设 |
| ②静置,向上层清液中滴加酚酞溶液 | 溶液 |
假设二成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com