
| A. | 生石灰与熟石灰都属于碱 | |
| B. | 酸就是有酸味的物质 | |
| C. | 碱就是有腐蚀性的物质 | |
| D. | 浓硫酸具有吸水性,在实验室中常用它做干燥剂 |
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 在食品包装袋中充入氮气以防腐 | |
| B. | 使用稀有气体制成霓虹灯 | |
| C. | 奶粉中含有三聚氰胺 | |
| D. | 净水器中用活性炭可以吸附水中的杂质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
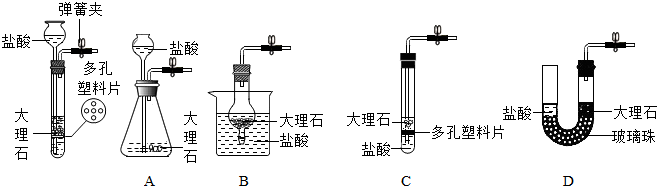
| 实验步骤 | 实验现象 | 实验结论 |
| 把生成的气体通入碳酸钠溶液中 | 产生气泡 | CO2中混有HCl气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 用元素符号或化学式表示 (1)-2价的氧元素$\stackrel{-2}{O}$; | (2)2个氧原子2O; |
| (3)氧单质O2; | (4)1个氧分子O2; |
| (5)4个二氧化碳分子4CO2; | (6)氯化钠NaCl; |
| (7)氢元素H; | (8)2个氢分子2H2; |
| (9)n个铁原子nFe. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
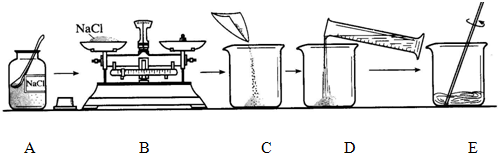
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com