
向盛有一定质量的NaCl和Na2SO4固体混合物的烧杯中加水,固体完全溶解后,再加入一定质量分数的BaCl2溶液至恰好完全反应,过滤烘干得到23.3g沉淀,经测定滤液中含有氯元素的质量为21.3g(不考虑过程中物质质量的损失),计算原固体混合物中NaCl的质量为
| A.5.85g | B.11.7g | C.14.2g | D.23.4g |
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:计算题
如图是某工业用食盐产品质量指标.为了测定其中氯化钠的质量分数,取100g该工业用食盐进行实验:①测得水的质量为3.36g;②用碳酸钠来测定杂质氯化钡的质量时,得到0.985g沉淀(化学方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl).
求:(1)100g该工业用食盐中含BaCl2的质量.
(2)请计算此工业用食盐中氯化钠的质量分数是多少?并判断该工业用食盐是否符合产品质量指标.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某化学兴趣小组的同学在实验室配制质量分数为20%的碳酸钠溶液,并完成有关实验。
(1)配制100g质量分数为20%的碳酸钠溶液。
①配制方法A、需要碳酸钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。配制方法B、若用40%的碳酸钠溶液稀释成100克20%碳酸钠溶液,则需取40%的碳酸钠溶液多少亳升?(密度为1.4克/毫升) (填答案)。
②配制溶质质量分数一定的碳酸钠溶液常按以下操作顺序进行。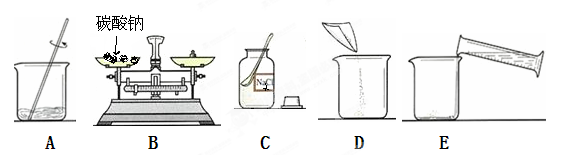
则用上图所示的序号表示正确配制该溶液的操作顺序为 。
③用托盘天平称量所需的碳酸钠时,发现托盘天平的指针偏向左盘,应 。
A.增加适量固体 B.减少适量固体
C.调节游码 D.添加砝码
④分析:以下原因可能导致配到的碳酸钠溶液溶质质量分数小于8%的是( )
A、固体中混有杂质
B、量水时仰视读数
C、配好后装入试剂瓶中时有少量液体洒出
D、量水时俯视读数
(2)取上述配制得到的20%的碳酸钠溶液53克,加入68.4克某浓度的稀盐酸后,恰好完全反应,求反应后所得溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
如图,表示镁、铜与其氧化物的质量关系。图线不重合的原因是 ( )
| A.镁和铜的密度不同 |
| B.与等质量的镁和铜化合的氧元素质量不同 |
| C.加热不充分,没有完全氧化 |
| D.实验的误差造成 |
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
某钢样品的含碳量为0.6%(杂质元素不考虑),若碳元素主要以Fe2C和Fe3C的形式存在,则该钢样品中Fe2C和Fe3C的质量分数(ω)范围是( )
| A.0.03%<ω<2% | B.0.6%<ω<0.87% |
| C.2.48%<ω<3.6% | D.6.2%<ω<9% |
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
点燃H2、O2和N2的混合气体20g,充分反应后生成18g水,则剩余的可能是( )
| A.O2和N2的混合气体2g | B.H2和N2的混合气体2g |
| C.H2、O2和N2的混合气体2g | D.2g N2 |
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
经过研究发现,对任何气体而言,6.02×1023个分子具有下列定量关系:①其质量在数值上等于该分子的相对分子质量,单位为克;②在压强为1.01×105Pa和0℃时其体积为22.4升。据此可知,32克二氧化硫的分子数为 个,含有的氧原子数为 个,在压强为1.01×105Pa和0℃时其体积为 升。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为xNaCl+2H2O xNaOH+H2↑+Cl2↑.在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g.已知:20℃时,NaC1的溶解度为36g.
xNaOH+H2↑+Cl2↑.在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g.已知:20℃时,NaC1的溶解度为36g.
请分析并计算回答:
(1)运用质量守恒定律可知上述反应中x= .
(2)通过计算,上述过程中同时产生H2的质量为 g.
(3)计算电解后剩余溶液中NaC1的质量分数(写出详细的计算过程,结果精确到0.1%).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com