
普通食盐的主要成份是NaCl和杂质,假设杂质不溶于水、受热不分解、与AgNO3不反应。王华同学测定普通食盐样品中氯化钠的质量分数时所进行的实验操作流程和实验数据如下图所示。
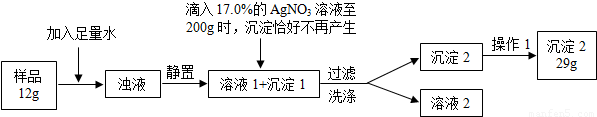
(实验中发生的化学反应方程式为:AgNO3+NaCl=AgCl↓+NaNO3)
请你完成空格和计算:
(1)王华进行操作1的目的是 _;
(2)求算样品中氯化钠的质量分数。(结果保留小数点后1位)
(1)干燥沉淀2;(2)样品中氯化钠的质量分数为97.5%
【解析】
试题分析:(1)过滤后沉淀2表面含有水,要得到沉淀2需除去表面的水,故操作1是将沉淀2进行干燥,除去水分,所起的作用是干燥沉淀2。
(2)由题意,食盐的主要成份是NaCl,氯化钠与加入的硝酸银溶液反应生成氯化银沉淀和硝酸钠,由参加反应的硝酸银溶液的质量200g、溶质的质量分数17.0%,利用溶质质量=溶液质量×溶质的质量分数,计算出所含溶质硝酸银的质量,进而由反应的化学方程式计算出样品中氯化钠的质量及质量分数200g17.0%的硝酸银溶液中含硝酸银的质量为200g×17.0%=34.0g,由于29g不溶性物质并不都是氯化银,所以不能用于求算氯化钠。设样品中氯化钠的质量为x
AgNO3+NaCl=AgCl↓+NaNO3
170 58.5
34.0g x
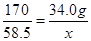
解得x=11.7g
样品中氯化钠的质量分数为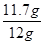 ×100%≈97.5%。
×100%≈97.5%。
答:(1)干燥沉淀2;(2)样品中氯化钠的质量分数为97.5%
考点:考查根据化学反应方程式的计算


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源:2013届江苏省南通市海安县九年级学业水平测试(一模)化学试卷(带解析) 题型:计算题
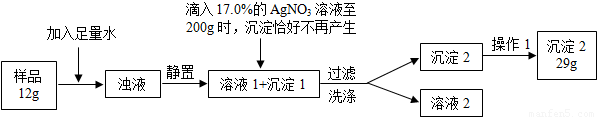
普通食盐的主要成份是NaCl和杂质,假设杂质不溶于水、受热不分解、与AgNO3不反应。王华同学测定普通食盐样品中氯化钠的质量分数时所进行的实验操作流程和实验数据如下图所示。
(实验中发生的化学反应方程式为:AgNO3 + NaCl =" AgCl↓+" NaNO3)
请你完成空格和计算:
⑴王华进行操作1的目的是 _;
⑵求算样品中氯化钠的质量分数。(结果保留小数点后1位)
查看答案和解析>>
科目:初中化学 来源: 题型:
普通食盐的主要成份是NaCl和杂质,假设杂质不溶于水、受热不分解、与AgNO3不反应。王华同学测定普通食盐样品中氯化钠的质量分数时所进行的实验操作流程和实验数据如下图所示。
(实验中发生的化学反应方程式为:AgNO3 + NaCl = AgCl↓+ NaNO3)
请你完成空格和计算:
⑴王华进行操作1的目的是 ▲ _;
⑵求算样品中氯化 钠的质量分数。(结果保留小数点后1位)
钠的质量分数。(结果保留小数点后1位)
查看答案和解析>>
科目:初中化学 来源:2013年江苏省南通市海安县中考化学一模试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com