
【题目】实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。某研究性学习小组发现一瓶未密闭的KOH固体,对其成分提出以下假设,并完成了实验探究。
假设1:只含KOH; 假设2:含KOH和K2CO3; 假设3:只含K2CO3
①成分中可能含有K2CO3的原因是(用化学方程式回答)______。
②取少量样品于试管中,加入足量稀盐酸,观察到______,说明假设2或假设3成立。
③进一步探究的过程如下:
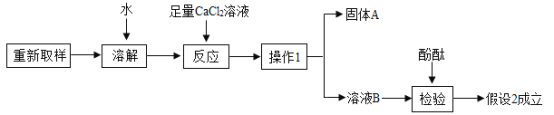
a“操作1”的名称是______;
b“固体A”的化学式是______;
c加入足量CaCl2溶液的作用是______;
【答案】2KOH+CO2=K2CO3+H2O 有气体产生 过滤 CaCO3 将碳酸钾完全反应,防止对氢氧化钾检验的干扰
【解析】
①氢氧化钾易吸收空气中的二氧化碳气体,产生碳酸钾和水,反应的方程式为:2KOH+CO2=K2CO3+H2O;故填:2KOH+CO2=K2CO3+H2O
②在检验是否变质时,只需检验碳酸钾存在,所以加入盐酸检验是否有气体产生,若产生气泡则说明含有碳酸钾,说明假设2或假设3成立;故填:有气体产生
③a“操作1”是将物质分成固体和液体,因此是过滤;故填:过滤
b “固体A”是变质后的碳酸钾和氯化钙反应产生的碳酸钙沉淀,化学式是为:CaCO3;故填:CaCO3
c在证明氢氧化钾部分变质时,因碳酸钾溶液也显碱性,因此加入足量的氯化钙先除去碳酸钾后再证明剩余溶液显碱性,故加入足量CaCl2溶液的作用是:将碳酸钾完全反应,防止对氢氧化钾检验的干扰;故填:将碳酸钾完全反应,防止对氢氧化钾检验的干扰


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:初中化学 来源: 题型:
【题目】测定石灰石中的碳酸钙的含量,取出2.5克石灰石样品,逐渐加入稀盐酸,充分反应后测得剩余固体质量与加入稀盐酸的质量关系如图所示.
(已知CaCO3+2HCl═CaCl2+H2O+CO2↑杂质不参与反应,也不溶于水)
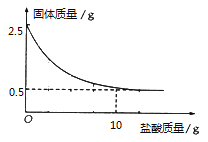
(1)石灰石样品中碳酸钙的质量是 g
(2)石灰石样品中碳酸钙的质量分数是
(3)计算稀盐酸溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国民间端午节有“挂艾草”的习俗。艾草中含有丰富的黄酮素(C15H10O2)有特殊的香味,人们用它来驱病、防蚊、辟邪,从分子的角度进行说明______。进行艾灸时可能会发生下列反应,含黄酮素222g的艾草与512g O2恰好完全反应,生成616g CO2和90g H2O和xg CO,x=______g;化学方程式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组对比实验,能达到实验目的是( )
A.研究温度对反应剧烈程度的影响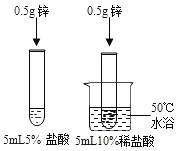
B.研究CO2气体是否与水发生反应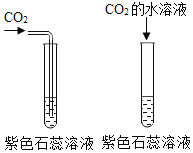
C.研究SO2是否能形成酸雨
D.研究白磷燃烧是否需要O2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属钛(Ti)的合金具有耐高温,耐腐蚀、强度高等性能,所以,钛合金广泛用于航空、航天工业及化学工业.工业上冶炼金属钛的过程是以钛矿石(主要成分为钛酸亚铁,化学式为FeTiO3)、焦炭、氯气为原料,在高温条件下制取TiCl4,其反应化学方程式为:2FeTiO3+6C+7Cl2![]() 2TiCl4+2X+6CO,然后用镁与TiCl4在高温条件下反应生成金属钛和氯化镁.请根据以上信息回答下列问题:
2TiCl4+2X+6CO,然后用镁与TiCl4在高温条件下反应生成金属钛和氯化镁.请根据以上信息回答下列问题:
(1)FeTiO3中钛元素的化合价为 价.
(2)在制备TiCl4的反应中,X的化学式为 .
(3)镁与TiCl4反应的化学方程式为: .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属与生活息息相关,认识金属的性质对我们至关重要,认真阅读,回答问题。
材料一:镓(Ga)是灰蓝色或银白色的金属,熔点很低,沸点很高。其化学性质与铝相似,能与氧气在加热时反应。金属镓广泛应用于半导体材料,光电子工业和微波通讯工业等领域。镓的原子结构示意图如图所示。
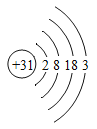
(1)镓的物理性质有_________________________。
(2)写出镓与氧气反应的化学方程式___________________________。
材料二:金属活动顺序在工农业生产和科学研究中有重要应用。现有铜、银、锌三种金属,某小组同学为了探究这三种金属的活动性,设计了以下实验:

(3)试管A中反应的化学方程式是_________________________,由实验A、B、C可推断出Ag、Zn、Cu三种金属的活动性由强到弱的顺序为_____________________。
(4)向C完全反应后的试管里加入一定质量的锌粒(如D试管)。D试管中一定会发生的反应是的化学方程式是________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究木炭在高温条件下还原氧化铜所生成的气体产物是什么,课外兴趣小组进行了如下实验探究:
(提出问题)生成的气体产物是什么?
(实验猜想)①猜想1:只有![]() ;猜想2:只有__________(填化学式);猜想3:含有
;猜想2:只有__________(填化学式);猜想3:含有![]() 和
和![]() 。若猜想1成立,木炭与氧化铜反应的化学方程式为______________________________。
。若猜想1成立,木炭与氧化铜反应的化学方程式为______________________________。
(实验探究)基于猜想3,根据![]() 和
和![]() 的性质,兴趣小组同学设计了如图装置进行探究。
的性质,兴趣小组同学设计了如图装置进行探究。
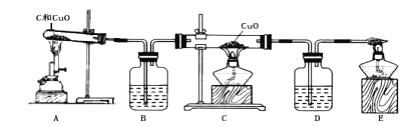
②若观察到__________________________________的现象,说明有一氧化碳气体生成。装置E的作用是________________________________________。
③装置B、D中都盛放了足量的澄清的石灰水,其中装置B的作用是______________。有同学认为:不需要装置D也能证明猜想3成立,你是否支持该同学的说法,并说明理由_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为甲、乙(均不含结晶水)两种固体物质的溶解度曲线。
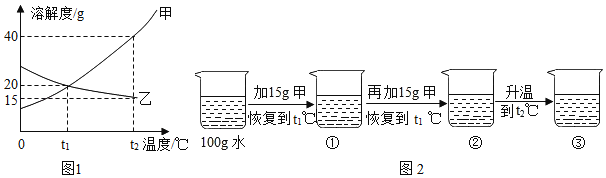
(I)溶解度随温度升高而增大的物质是_____(填“甲”或“乙”);t1℃时,甲的溶解度_____(填“大于”“小于”或“等于”)乙的溶解度。
(II)某同学在t1℃时开始进行如图2实验,得到相应的溶液①~③.在溶液①~③中属于饱和溶液的是_____(填序号)、溶质质量分数最大的是_____(填序号)。
(III)t2℃时280g甲的饱和溶液中所含甲的质量为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
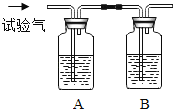
【题目】生活生产中CH4、H2和CO均可燃烧,为了确定三种可燃性气体:分别将它们在氧气中燃烧,把燃烧后生成的气体依次通过A、B两个洗气瓶,回答下列问题:注:装置A中的是浓硫酸,作用吸水:B中的是氢氧化钠溶液,作用是吸收二氧化碳气体.
(1)若装置A的质量增加,B的质量不变,则试验气是_____;
(2)若装置A的质量不变,B的质量增加,则试验气是_____.
(3)CH4的燃烧产物会使A的质量增加,B的质量_____〔填“增加”或“不变”).
(4)若将上述A瓶中改装氢氧化钠溶液、B瓶中改装浓硫酸,进行实验.有同学提出,B瓶中的质量始终都有可能增加,不能判断哪种可燃气体.请你评价他的说法是否合理,理由是_____.
(5)如果将上述三种气体中任取两种混合,燃烧后产物通过A、B两个洗气瓶,发现A瓶质量增加的数值比B瓶大,则实验所取的两种气体可能是_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com