【答案】
分析:(1)聚氨酯泡沫塑料属于有机合成材料,具有可燃性;
(2)可燃物燃烧的条件是:与氧气接触,温度达到可燃物的着火点;
(3)氢氧化镁分解能生成氧化镁和水;
(4)实验时,应该先检验装置的气密性,然后再加入药品;
根据化学方程式可以进行相关方面的计算.
解答:解:(1)聚氨酯泡沫塑料属于合成材料,具有可燃性.故填:合成材料;可燃性.
(2)燃着的烟花在引发这场火灾中所起的作用是使聚氨酯泡沫塑料温度达到着火点.故填:使聚氨酯泡沫塑料温度达到着火点.
(3)氢氧化镁受热分解的化学方程式为:Mg(OH)
2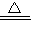
MgO+H
2O.
氢氧化镁能作阻燃剂的原因可能有:氢氧化镁受热开始分解出水蒸气,同时生成耐高温的氧化镁固体,将可燃物与空气隔离.故填:氢氧化镁受热开始分解出水蒸气,同时生成耐高温的氧化镁固体,将可燃物与空气隔离.
(4)①样品取用的量需要一定的控制,这是因为注射器最大量程为20mL.故填:注射器最大量程为20mL.
②实验时,应该先检验装置的气密性,然后再加入药品.故填:b a c d.
③最后测得的气体的体积应该就是量筒中水的体积数.故填:量筒中水的体积.
④理由是反应生成的氨气溶于水所致.故填:反应生成的氨气溶于水所致.
⑤X可以选用的物质是植物油,它的作用是防止氨气溶于水.故填:植物油;防止氨气溶于水.
⑥实验中广口瓶内原有的空气对实验结果没有影响.故填:没有.
⑦若观察到锥形瓶中还有固体,则样品中肯定含有的杂质是碳.故填:碳.
⑧解:设AlN质量为x
AlN+NaOH+H
2O=NaAlO
2+NH
3↑
41 17
x 0.5 L×0.68g/L
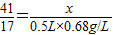
解得:x=0.82g<1g-0.08=0.92g
故该样品中还含有另一种杂质能与氢氧化钠溶液反应的杂质
点评:本题主要考查根据化学方程式计算和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

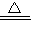 MgO+H2O.
MgO+H2O.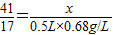


 作业辅导系列答案
作业辅导系列答案 (2011?丹阳市二模)学好化学可以避免生活中的盲目行为.日本大地震造成的核泄露事故使“吃碘防辐射”之说成为热点话题,并在社会上造成短暂的“盐荒”.其实我国加碘盐产量和储备都非常充足.右图是某品牌加碘盐的标签,下列有关说法不正确的是( )
(2011?丹阳市二模)学好化学可以避免生活中的盲目行为.日本大地震造成的核泄露事故使“吃碘防辐射”之说成为热点话题,并在社会上造成短暂的“盐荒”.其实我国加碘盐产量和储备都非常充足.右图是某品牌加碘盐的标签,下列有关说法不正确的是( )