
 现有含氯化钠杂质的氢氧化钠10g,逐渐加入溶质质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示:
现有含氯化钠杂质的氢氧化钠10g,逐渐加入溶质质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示:分析 当反应后的溶液的PH=7时表示盐酸和氢氧化钠恰好反应,由图看出恰好反应时反应了100g盐酸;根据反应的盐酸的质量,利用化学方程式求出参加反应的氢氧化钠的质量,进而求出氯化钠溶液的质量分数.
解答 解:(1)根据曲线可以看出,A点pH>7,说明此时有过量的氢氧化钠、有盐酸与氢氧化钠反应生成的氯化钠,故A点时溶液中所含的阴离子是OH-、Cl-;
(2)B点时盐酸与氢氧化钠恰好完全反应,故设参加反应的氢氧化钠的质量为x,生成的氯化钠为y.
NaOH+HCl═NaCl+H2O
40 36.5 58.5
x 100g×7.3% y
则$\frac{40}{36.5}=\frac{x}{100g×7.3%}$,$\frac{36.5}{58.5}=\frac{100g×7.3%}{y}$,解得x=8g,y=11.7g.
故B点时所得溶液中溶质的质量分数是$\frac{11.7g+(10g-8g)}{10g+100g}×100%$≈12.5%
故答案为:
(1)OH-、Cl-;(2)12.5%.
点评 此题是一道结合图象的计算题,解题时找到PH=7的恰好反应点,并利用化学方程式的计算进行解决是解题的突破口.


科目:初中化学 来源: 题型:推断题
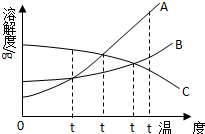 如图是A、B、C三种物质的溶解度曲线:
如图是A、B、C三种物质的溶解度曲线:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
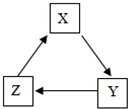 下列各组物质间不能通过一步反应就能实现如图转化的是( )
下列各组物质间不能通过一步反应就能实现如图转化的是( )| 选项 | X | Y | Z |
| A | H2SO4 | H2 | H2O |
| B | CuSO4 | CuCl2 | Cu(OH)2 |
| C | H2O | H2 | CO2 |
| D | Cu | CuO | CuSO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NH4H2PO4 | B. | CO(NH2)2 | C. | K2CO3 | D. | Ca3(PO4)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 墙内开花墙外香是因为分子在不断运动 | |
| B. | 热胀冷缩是因为分子大小随温度而改变 | |
| C. | 蔗糖溶解是因为分子很小 | |
| D. | 气体易被压缩是因为气体分子间间隔很小 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实 验 步 骤 | 实 验 现 象 | 结 论 |
| ①取一定量的合金粉末,加过量的20%的NaOH溶液,充分反应后过滤,滤渣备用 | 粉末部分溶解,并有无色气体放出 | 合金中一定含有铝 |
| ②取步骤①所得滤渣,加过量20%的H2SO4溶液, 充分反应 | 滤渣部分溶解,并有无色气体放出,溶液呈浅绿色 | 合金中一定含有铁,铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com