
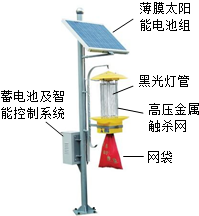
 如图是一个太阳能黑光灯灭虫装置,上方的薄膜太阳能电池组将太阳能转化成电能,为诱虫的黑光灯及高压金属触杀网供电.
如图是一个太阳能黑光灯灭虫装置,上方的薄膜太阳能电池组将太阳能转化成电能,为诱虫的黑光灯及高压金属触杀网供电.分析 (1)此题考查的知识点是害虫抗药性的形成.解答时可以从自然选择和抗药性形成的过程方面来切入.
(2)土壤污染是指土壤中积累有毒、有害物质,引起对植物生长的危害,或者残留在农作物中进入食物链而危害人体健康.
(3)根据化学反应的方程式进行分析.
解答 解:(1)达尔文把在生存斗争中,适者生存、不适者被淘汰的过程叫做自然选择.遗传变异是生物进化的基础,首先害虫的抗药性存在着变异.有的抗药性强,有的抗药性弱.使用农药时,把抗药性弱的害虫杀死,这叫不适者被淘汰;抗药性强的害虫活下来,这叫适者生存.活下来的抗药性强的害虫,繁殖的后代有的抗药性强,有的抗药性弱,在使用农药时,又把抗药性弱的害虫杀死,抗药性强的害虫活下来.这样经过若干代的反复选择.最终活下来的害虫大多是抗药性强的害虫.在使用同等剂量的农药时,就不能起到很好的杀虫作用,导致害虫产生抗药性.
(2)溶解在土壤中的镉会被植物吸收,说明有毒物质会随着食物链的传递积累,最终危害人的健康.
(3)由化学方程式CdSO4+Na2S═CdS↓+NaSO4可知,通过该反应把可溶性的CdSO4转化为不溶性的CdS.
故答案为:(1)自然选择;
(2)食物链;
(3)把可溶性的CdSO4转化为不溶性的CdS.
点评 本题综合能力较强,考查的知识点很多,有一定难度,这要求学生多读多了解物理知识在生活中的应用情况.


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 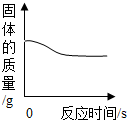 加热木炭粉与氧化铜的混合物 | B. | 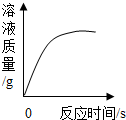 锌粒加入一定量的稀盐酸中 | ||
| C. | 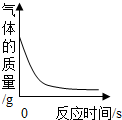 点燃的硫伸入装满氧气的集气瓶中 | D. | 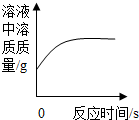 一定量稀硫酸中滴加氢氧化钡溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | O | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | O.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
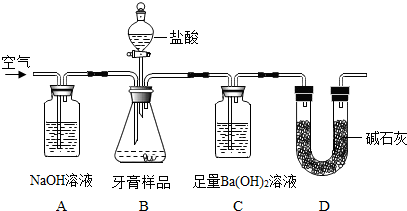
| 实验次数 | 样品质量(g) | 所用盐酸质量(g) | 所得沉淀质量(g) |
| 第一次 | 8.00 | 50 | 1.95 |
| 第二次 | 8.00 | 50 | 1.98 |
| 第三次 | 8.00 | 50 | 1.96 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫酸厂的废气直接排放 | B. | 汽车尾气直接排放 | ||
| C. | 含硫煤的燃烧 | D. | 建筑工地的尘土飞扬 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
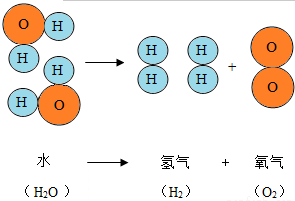 如图是水分子分解示意图,下列说法正确的是( )
如图是水分子分解示意图,下列说法正确的是( )查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
| A. | 表中m的值为2.8 | |
| B. | X中氧元素的质量为1.6g | |
| C. | 增加氧气的量可以减少X的生成 | |
| D. | 物质X一定含有1.2g碳元素,可能含有氢元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
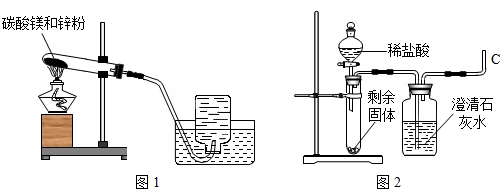
| 序号 | 实验操作 | 实验现象 |
| ① | 收集两瓶气体,盖好玻璃片,停止加热,向其中一瓶迅速倒入少量澄清石灰水,盖好振荡. | 无明显现象. |
| ② | 将另一瓶气体点燃,待火焰熄灭后,迅速倒入少量澄清石灰水,盖好振荡. | 气体安静燃烧,火焰呈蓝色,澄清石灰水变浑浊. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com