
| A. | M的金属活动性比Ag强 | B. | 金属M可能是铝 | ||
| C. | 该反应属于复分解反应 | D. | 该反应前后M的化合价发生了改变 |
分析 根据题意,金属M能与硝酸银反应置换出银,说明R的活动性比银强,再结合反应的方程式进行有关问题的分析判断
解答 解:A、由于金属M能与硝酸银反应置换出银,说明M的金属活动性比银强,故A说法正确;
B、如果M是铝,铝与硝酸银反应生成银和硝酸铝,由于硝酸根-1价,铝+3价,所以硝酸铝写为:Al(NO3)3,图示中M是+2价,所以M不能是铝,故B说法错误;
C、该反应有一种单质和化合物反应,生成了另一种单质和化合物,属于置换反应.故C说法错误;
D、反应前M是单质化合价为0,反应后生成了M(NO3)2M的化合价是+2价,化合价发生了改变,故D说法正确.
故选:BC.
点评 金属单质能置换出盐中的金属,说明组成单质的金属元素的活动性比盐中金属元素的活动性强.


科目:初中化学 来源: 题型:选择题
| 废液来源 | 甲组 | 乙组 |
| 检测方法与结果 | 观察废液呈无色 | 观察废液呈红色 |
| A. | 甲组废液中一定含有稀盐酸或稀硫酸 | |
| B. | 乙组废液中一定含有氢氧化钠、氯化钠、硫酸钠 | |
| C. | 甲组废液可直接排放,乙组处理后再排放 | |
| D. | 如将两组的废液合并在一起,如溶液呈无色,混合液可直接排放 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
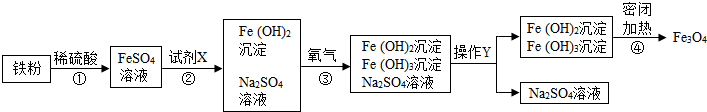
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 打开盛有浓硫酸的试剂瓶瓶盖,瓶口上方出现大量白雾 | |
| B. | 向稀盐酸中滴加适量紫色的石蕊试液,溶液的颜色由无色变成蓝色 | |
| C. | 分别点燃一小块棉纤维和羊毛纤维,都产生了烧焦羽毛的气味 | |
| D. | 红磷在空气中燃烧产生大量的白烟 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
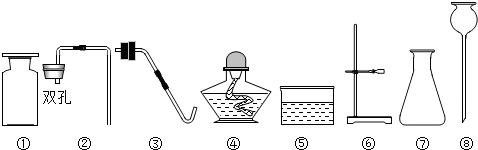
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
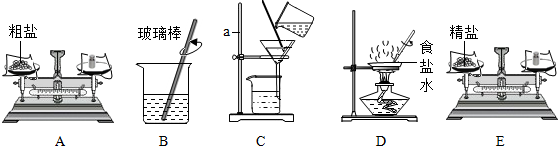
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com