
分析 (1)根据浓盐酸配稀盐酸的步骤解答;根据浓盐酸配稀盐酸溶质不变列等式即可,根据溶液配制需要的仪器考虑;根据过滤操作使用的仪器和玻璃棒的作用考虑;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.根据高锰酸钾制氧气需用的仪器考虑本题.
解答 解:(1)①浓盐酸配稀盐酸的步骤是计算、量取、溶解;
②设需要浓盐酸的体积为V则:V×1.18g/cm-3×37%=200g×10%,解得V=$\frac{200g×10%}{1.18g/c{m}^{3}×37%}$mL,
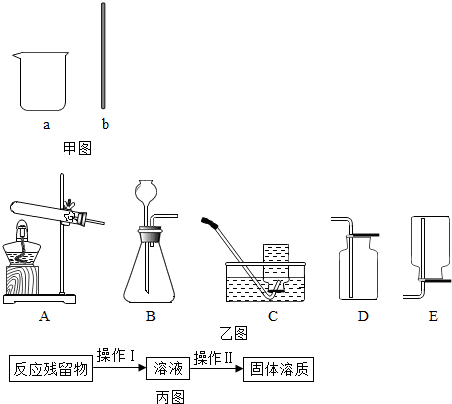
③配制稀盐酸用到的仪器有:烧杯、玻璃棒、量筒、胶头滴管;
(2)①实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;发生反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;实验结束,从反应残留物中提取固体溶质时,按如丙图流程操作.此流程中,操作Ⅰ的名称是过滤,操作Ⅱ的名称是蒸发;
②如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
答案:
(1)①量取; ②$\frac{200g×10%}{1.18g/c{m}^{3}×37%}$;③烧杯;玻璃棒、量筒、胶头滴管;
(2)①BD;CaCO3+2HCl=CaCl2+H2O+CO2↑; 过滤;蒸发;②2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
点评 通过回答本题要知道浓盐酸配稀盐酸时溶质不变列等式计算待求量,有体积出现时别忘了用体积乘以密度算出质量,再用质量乘以溶质质量分数,千万别直接用体积乘以溶质质量分数.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:选择题
| A. | Ni | B. | NI | C. | N | D. | Na |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验操作 | 现象 | 结论 | |
| A | 向醋酸中加入氢氧化钠溶液 | 无明显现象 | 二者之间不反应 |
| B | 向溶质质量分数为5%的过氧化氢溶液中加入少量氧化铜粉末 | 有大量气泡产生 | 氧化铜起催化作用 |
| C | 将两根铁丝分别深入到硫酸铜溶液和硝酸银溶液中 | 两根铁丝上均有固体附着 | 金属的活动性为Fe>Cu>Ag |
| D | 用导管分别对准浸没在冷水和热水中的白磷通气 | 热水中的白磷燃烧,冷水中的白磷不燃烧 | 燃烧的条件之一是温度达到着火点 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | SO42-、NO3-、K+、H+ | B. | Na+、Cl-、SO42-、Al3+ | ||
| C. | Cl-、NO3-、K+、Na+ | D. | Ag+、Cl-、CO32-、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com