
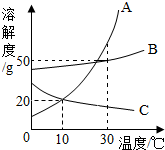
 如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线,下列说法不正确的是( )| A. | 30℃时,A、B、C三种物质的溶解度曲线由大到小的顺序是:A>B>C | |
| B. | 30℃时,A、B、C三种饱和溶液同时降温到10℃,所得溶液中溶质分数由大到小的顺序是:B>A>C | |
| C. | 10℃时,A、B、C三种饱和溶液同时升温到30℃,所得溶液中溶质分数由大到小的顺序是:B>A>C | |
| D. | 30℃时,A、B、C三种饱和溶液同时降温到10℃,析出的晶体质量大到小的顺序一定是:A>B>C |
分析 根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
溶液中溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%.
解答 解:A、由溶解度曲线可知,30℃时,A、B、C三种物质的溶解度曲线由大到小的顺序是:A>B>C,该选项说法正确;
B、10℃时,B的溶解度大于A的溶解度,因此A的质量分数小于B的质量分数,A在10℃时的溶解度大于C在30℃时的溶解度,因此A的质量分数大于C的质量分数,所得溶液中溶质分数由大到小的顺序是:B>A>C,该选项说法正确;
C、10℃时,B的溶解度大于A的溶解度,A和C的溶解度相等,升温到30℃时,A、B变成不饱和溶液,质量分数不变,C仍然是饱和溶液,由于析出固体,质量分数减小,因此A、B、C三种饱和溶液同时升温到30℃时,所得溶液中溶质分数由大到小的顺序是:B>A>C,该选项说法正确;
D、由于不知道饱和溶液的质量,因此无法比较析出固体质量的大小,该选项说法不正确.
故选:D.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


科目:初中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 2014年4月14日,科学家约翰•帕特森向人作展示了一款真正意义上的原子手表,它内置了一个芯片级的铯原子钟,每1000年仅有1秒的误差,如图为铯的原子结构示意图,下列说法不正确的是( )
2014年4月14日,科学家约翰•帕特森向人作展示了一款真正意义上的原子手表,它内置了一个芯片级的铯原子钟,每1000年仅有1秒的误差,如图为铯的原子结构示意图,下列说法不正确的是( )| A. | 该原子的核外有55个电子 | |
| B. | 该原子的核内有55个中子 | |
| C. | 该原子的次外层上有8个电子 | |
| D. | 该原子在化学式反应中容易失去1个电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 A、B是两种常见的单质.甲、乙、丙是初中常见的三种化合物,它们都由两种元素组成,这些单质和化合物之间存在如下关系:(图中“→”表示物质间存在的转化关系,部分生成物已略去).
A、B是两种常见的单质.甲、乙、丙是初中常见的三种化合物,它们都由两种元素组成,这些单质和化合物之间存在如下关系:(图中“→”表示物质间存在的转化关系,部分生成物已略去).查看答案和解析>>
科目:初中化学 来源: 题型:填空题
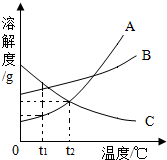 如图A、B、C为三种物质的溶解度曲线,据图回答:
如图A、B、C为三种物质的溶解度曲线,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
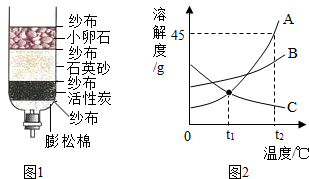 2015年整个潍坊地区干旱少雨,影响了我们的生活.水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
2015年整个潍坊地区干旱少雨,影响了我们的生活.水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com