
����Ŀ����һ�ձ���ʢ��22.3g Na2CO3��NaCl��ɵĹ������������ˮ�ܽ⣬�Ƴ���Һ���������μ�������������Ϊ10%��ϡ���ᣬ�ų��������������������ϡ�����������ϵ������ͼ��ʾ��
��1�����μ���73gϡ����ʱ���ų������������Ϊ g��
��2�����μ�ϡ������ͼ��B��ʱ���ձ�����Һ��������ǣ�д��ѧʽ�� ��
��3�����μ���73gϡ����ʱ����A��ʱ�����ձ���Ϊ��������Һ����ͨ��������������������ʵ�������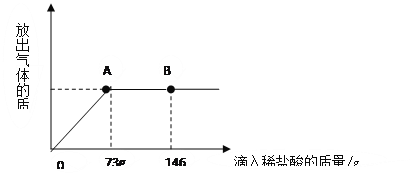
���𰸡���1��4.4���˿�2�֣�
��2��NaCl��HCl ���˿�2�֣�
��3������С��6�֣�
�⣺73g10%��ϡ�����к�HCl�������ǣ�
73g��10%=7.3g
��μӷ�Ӧ��̼���Ƶ�����Ϊx����Ӧ���ɵ��Ȼ��Ƶ�����Ϊy
Na2CO3+ 2HCl =" 2NaCl" + CO2�� + H2O
106 73 117
x 7.3g y
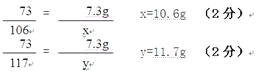
�ձ��ﲻ������Һ�����ʵ�����Ϊ�� 117.g + (22.3g��10.6g) =" 23.4g" ��2�֣�
�𣺣��ԣ�
����������������� ��1�����ݣ�3�������֪���������������Ϊ4.4 g
��2����ͼ��֪A�㴦��̼���ƺ����ᷴӦ��ȫ�������Ȼ��ƣ��μ����ᵽB����������� �ձ�����Һ��������ΪNaCl ��HCl
��3���⣺73g10%��ϡ�����к�HCl�������ǣ�73g��10%=7.3g
��μӷ�Ӧ��̼���Ƶ�����Ϊx����Ӧ���ɵ��Ȼ��Ƶ�����Ϊy���ɵĶ�����̼������Ϊz
Na2CO3+ 2HCl="==2NaCl" + CO2�� + H2O
106 73 117 44
x 7.3g y z
���x=10.6g y=11.7g z=4.4g
�ձ��ﲻ������Һ�����ʵ�����Ϊ�� 117.g + (22.3g-10.6g) = 23.4g


 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���С���ͬѧ������������Һ�������������кͷ�Ӧ��ʵ��ʱ�����ձ��е�ϡ�����������������Һһ����������ǵμ�ָʾ������ˣ�����ֹͣ�μ�����������Һ�������ձ�����Һ�е����ʳɷֽ���̽��
��������⣩���ձ�����Һ�е�������ʲô��
��������룩��������������CaCl2��Ca��OH��2����������_____������������CaCl2��HCl
���������ϣ��Ȼ�����Һ�����ԡ�
��ʵ��̽����
ʵ�鲽�� | ʵ������ | ���� |
ȡ�����ձ�����Һ���Թ��У����뼸�η�̪��Һ | _____ | ������������ |
ȡ�����ձ�����Һ���Թ� ����μ���Na2CO3��Һ | _____ | ���������� |
_____ | ���������� |
����˼����1���ڷ�����ѧ��Ӧ���������ʳɷ�ʱ�����������������Ҫ����_____��
��2������������ȷ��Ҫ�����ձ�����Һʹ������ֻ����CaCl2��Ӧ���ձ��м��������_____����ѧʽ����
��3����֤�ձ�����Һ�е����ʺ���HCl�������Ϸ����⣬������Щ���ʻ��߷�������ʹ��Ҳ����ɸ�ʵ��_____��
A��pH��ֽ B��þ�� C����鵼���� D��ͭƬ
����չ���죩��ע�⣺����ԣ���չ���죩����4�֣���ѧ�Ծ��ֲܷ�����60�֡���
��1���ڽ�������кͷ�Ӧʵ��Ĺ����У��о���С��ȡһ������ϡ���ᣬ������ٵμ�����������Һ����pH���¶ȵ��Ӵ�����ʵʱ��õ�pH���¶����ߣ���ͼ������ͼ��õ�����ʶ��
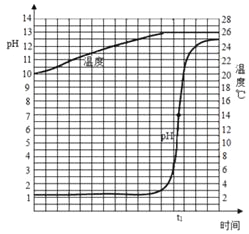
���������_____��_____��
��2�������ǻ�ѧ�����������Ҫ��ɲ��֣�Ҳ�ǻ�ѧ����������������IJ��֣������ӽ���ʶ�Ϳ��������������о���ѧӦ���յ���Ҫ˼ά�������Դ��۽Ƕȷ�������кͷ�Ӧ��ʵ����_____�����кͷ�Ӧʵ�ʿ���֪������������ˮ��Һ�в��ܹ��棬����д��һ�鲻�ܹ��������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20��ʱ������������a��b���ֲ����ᾧˮ�Ĺ������ʣ��ֱ���뵽ʢ��100gˮ���ձ��У���ֽ����������ͼ1��Ȼ�����µ�50��ʱ��������ͼ2��a��b�������ʵ��ܽ��������ͼ3������һ���̿�֪��������
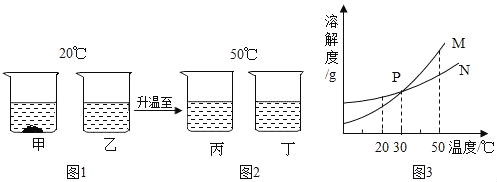
A. 30��ʱa��b��Һ�����������������
B. 40��ʱa��b��Һ��������������С���Ƚ�
C. ��20�浽50�棬b��Һ������������
D. ͼ3�б�ʾa���ܽ��������N
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڹ�ҵ��������Ҫ����;���Ի�������Ҫ�ɷ�ΪFeS2��Ϊԭ�����������ԭ�����������̿ɼ�ʾ���£�FeS2![]() SO2
SO2![]()
![]() H2SO4
H2SO4
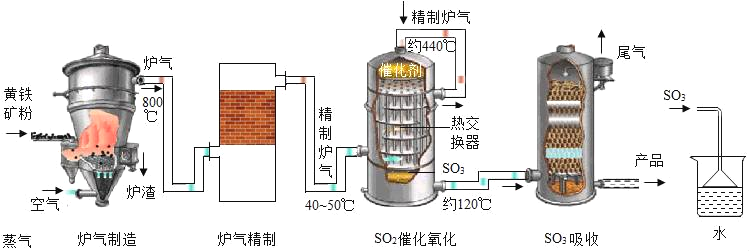
��1����ҵ���������н���ʯ�����Լ�������װ����Һ�����϶����γ�����״��Ŀ����_____��
��2����ʵ����ģ��������ʱ����ͼװ���������������˴ﵽ�빤ҵ����ͬ��Ŀ���⣬�����ܿ��ǵ�������_____��
��3����ҵ�ϳ�����ʯ��������β���еĶ���������д����Ӧ�Ļ�ѧ����ʽ_____������ʾ����������һ����CaSO3��
��4��ʵ�����г���Ũ����������ϡ���ᡣϡ��ʱ����ȷ�����ǣ�_____�����ò��������Ͻ��衣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ҹ�������������������������������Ҫԭ��֮һ��ȼú������������ȼú�����������к��ж�������ֱ���ŷŻ���Ⱦ������ij����С�����ú�ˮ��ȥ���������乤�����̼�ͼ��
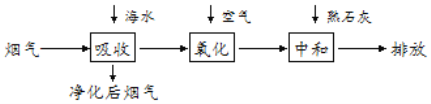
��ش��������⣺
��1����������Ի�����ɵ���Ⱦ���γ�_____��
��2��Ϊ���о������ʣ����������ѳ�ȥ�Ķ����������ռ�ܶ����������İٷֱȣ� ���¶ȡ�������SO2Ũ�ȵĹ�ϵ�����ǽ�����̽��ʵ�顣ʵ�������£�
ʵ����� | �¶�/�� | ������SO2Ũ��/10��2gL��1 | ������ |
�� | 23 | 2.5% | 99.5 |
�� | 23 | 3.2% | 97.1 |
�� | 40 | 2.5% | 94.3 |
�ɱ���ʵ�����ݿɵó��Ľ�����_____��
��3��Ŀǰ��������ϩ��C2H4����������Ϻ���Cu+�����³�ȥ������������һ�ֹ��嵥�ʡ�һ����ʹ����ʯ��ˮ����ǵ������һ��Һ�塣
��������л�ѧ����ʽ��C2H4+SO2+2O2�T_____��
����Ӧ������Cu+��������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ȤС���ͬѧ��������п�����뵽Ũ�����У������д��������ݷų������Ƕ�����ijɷֽ�����̽����
��������⣩п������Ũ��������ɵ�������ʲô��
���������ϣ���Ũ��������п��Ӧ����������������Ҳ�������������
��SO2�д̼�����ζ��������ˮ����ʹƷ�죨һ�ֺ�ɫɫ�أ���Һ��ɫ��
��SO2��CO2������������Һ��Ӧԭ����ͬ���ҷ�Ӧǰ����Ԫ�ػ��ϼ۲��䡣
��������룩�ף�������H2��
�ң������ǣ�SO2��
����������_____��
��ʵ��̽����Ϊ����֤�������룬ͬѧ������ʦ��ָ�����������ͼ��װ�ã����ּг�������ȥ������ÿ���ܷ����ķ�Ӧ����ȫ���У�����̽����
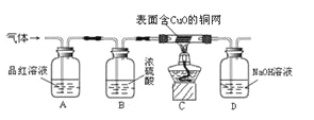
��1��ʵ�鿪ʼ�۲쵽A��Ʒ����Һ��ɫ��֤�������к���_____��
��2��Bװ�õ�����������Ũ�����_____�ԡ�
��3��Cװ���ڵ�ȼ�ƾ��Ƽ���֮ǰӦ��ͨһ��ʱ������壬Ŀ����_____������һ��ʱ��۲쵽_____������֤�������к���H2��
��4��Dװ�õ�Ŀ��������β���е�SO2����ֹ��ɿ�����Ⱦ������д��Dƿ�з�����Ӧ�Ļ�ѧ����ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼����ϩ��(C3H4O3)������﮵�ص��Һ�������й�̼����ϩ����˵����ȷ����
A. ̼����ϩ������Է�������Ϊ(12��3+1��4+16��3)g
B. ̼����ϩ����C��H��O����Ԫ�ص�������Ϊ12:1:16
C. ̼����ϩ����C��H��O����ԭ�ӵĸ�����Ϊ3:4:3
D. ̼����ϩ����̼Ԫ�ص���������= ![]() ��100%
��100%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ȼ�գ�chemical��looping combustion�����µ�ȼ�������ȼ�ϲ�ֱ��������Ӵ�ȼ�գ������������壨��CaSO4�ȣ���������Ӧ��֮���ѭ����ʵ��ȼ�ϵ�ȼ�գ�������ͼ����ش��������⣺

��1��������Ӧ������Ҫ�������Ϸ�Ӧ����ѧ����ʽΪ_____����Ӧ����Ԫ�صĻ��ϼ�_____������ߡ��� �͡�����
��2��ȼ�Ϸ�Ӧ���У�CO��CaSO4�����ķ�Ӧ�Ļ�ѧ����ʽΪ_____��
��3��ͨ��ȼ�Ϸ�Ӧ���Ƶø���CO2��H2O��������Ϊ��ȡ������CO2�����õ��������뷽����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��t1��ʱ����������������غ͚⻯�طֱ���뵽��ʢ��100gˮ�������ձ���,��ֽ����������ͼ1��ʾ������غ͚⻯�صĬ����������ͼ2��ʾ��������˵����ȷ����
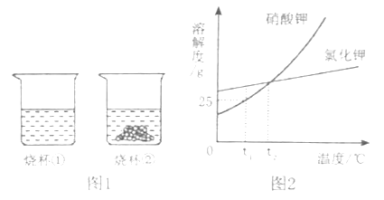
A���ձ�������Һһ���Dz����ͬ�Һ
B���ձ�������Һ���������Һ
C���ձ�������Һ���µ�t2��ʱ,�ձ��ײ����в������ʲ��ܽ�
D�����ձ������ձ�������Һ�����µ�t2��ʱ,���ʵ������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com