
【题目】有一包白色粉末可能由NaCl、NaNO3、MgCl2、CuSO4中的一种或多种物质组成。小明为了探究其成分,设计并完成了如下图所示的实验。

根据以上实验,回答:
(1)操作①是_________
(2)原固体粉末中一定没有的成分是_______。
(3)上述实验____(填‘能’或‘不能’)确定原固体粉末中含有NaCl。
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:初中化学 来源: 题型:
【题目】实验室用下图装置制取CO2并研究CO2性质。将稀盐酸推入C装置中。
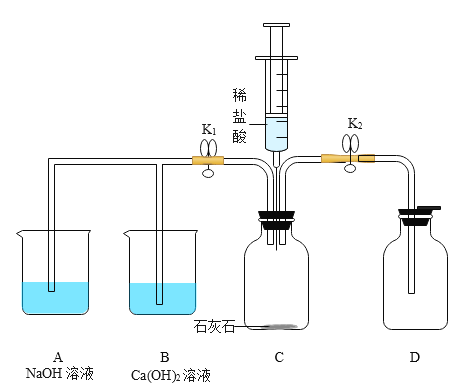
(1)打开K2,用D装置收集CO2的依据是_____
(2)关闭K2打开K1,其中一个烧杯中产生白色沉淀,写出该反应的化学方程式____;另一烧杯中无明显现象,为了证明反应的发生可以再向该烧杯中滴加适量的_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示装置,结合所学化学知识回答下列问题:
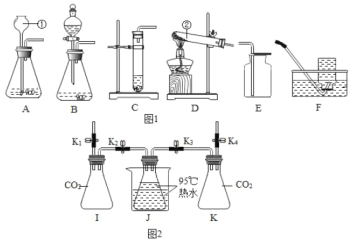
(1)写出图1中标号仪器的名称:①________。
(2)实验室用高锰酸钾制取氧气时,发生装置应选用____(填字母);其反应的化学方程式为________。如果改用氯酸钾和二氧化锰制取氧气,反应前后固体中二氧化锰的质量分数_____(填“增大”、“减小”或“不变”)。
(3)实验室制取少量二氧化碳时,发生装置最好选用____(填字母,下同),收集装置选用___,常用此收集方法的原因是________。
(4)CO2能与NaOH发生反应。
[实验过程]检查装置气密性,如图2所示连接好装置,进行实验。
序号 | 操作步骤 | 实验现象 |
Ⅰ | 打开弹簧夹K1,关闭弹簧夹K2、K3、K4.将20mL水注入锥形瓶I中,关闭弹簧夹K1,振荡瓶J,打开弹簧夹K2. | 无明显现象 |
Ⅱ | 关闭弹簧夹K2,打开弹簧夹K4,将20mL 稀NaOH溶液注入锥形瓶K中,关闭弹簧夹K4,振荡瓶J,打开弹簧夹K3. | 锥形瓶J中的热水剧烈沸腾 |
[实验分析]锥形瓶J的热水剧烈沸腾的原因是____________。
[实验反思]有观点认为只需要进行实验操作Ⅱ,即可说明CO2与NaOH发生反应。
你对该观点的看法是___________(选填“赞同”或“不赞同”),理由是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧乙酸对细菌和病毒具有高效、快速杀灭作用,广泛应用于环境的消毒。如图为过氧乙酸的分子结构图(其中![]() 代表碳原子,
代表碳原子,![]() 代表氢原子,
代表氢原子,![]() 代表氧原子),下列有关说法正确的是
代表氧原子),下列有关说法正确的是
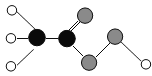
A.过氧乙酸的化学式是CH3COOOH(或C2H4O3)
B.过氧乙酸是由碳、氢、氧三种元素构成的
C.过氧乙酸中碳、氢、氧三种元素的质量比是12: 1: 16
D.过氧乙酸中氢元素的质量分数最大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学实验小组对“影响石灰石与盐酸反应速率的因素一一盐酸的浓度 和石灰石的颗粒大小等”进行了如下实验探究,请你参与。
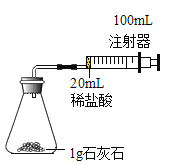
进行实验 室温下,选用20mL不同浓度的盐酸(4%和6%)分别与lg颗粒状或块状的石灰石进行实验( 固定夹持仪器略去)。
(1)石灰石与盐酸反应的化学方程式为___________。
(2)按如图所示装置进行实验,在装药品前应检查该装置的气密性,具体的做法是连接好仪器,拉动注射器活塞,然后松开手,若______,说明装置气密性良好。开始实验时,应将20mL稀盐酸_____(选填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
处理数据 实验小组进行实验后,获得的相关实验数据如表所示:
实验编号 | 盐酸的溶质质量分数(均取20 mL) | 石灰石固体形状(均取1g) | 二氧化碳的体积/mL(均收集前30 s的气体) |
a | 4% | 颗粒 | 64.0 |
b | 4% | 块状 | 40.4 |
c | 6% | 颗粒 | 98.2 |
d | 6% | 块状 | 65.3 |
(3)①要比较不同浓度的盐酸对反应速率的影响,可选择的实验编号是_____(写一组), 由此可得到的结论是_________。
②从上述实验得出石灰石的颗粒大小对反应速率影响的结论是_________。
(4)如下表是实验时记录生成的二氧化碳气体的体积和对应时间的一组实验数据(每间隔4s读数一次):
时间/s | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
气体体积/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
从上表数据可以分析得出,到20s后反应速率逐渐变慢,其原因是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某些元素的原子核外电子的分布情况,请回答下列问题:
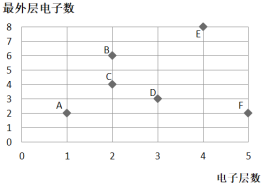
(1)具有相对稳定结构的是________和E(填字母);
(2)属于金属元素的是_______,D形成的离子符号为_______;
(3)若F的元素符号为Sr,则B、C、F三种元素形成的化合物的化学式为__________;
(4)下图是某个反应的微观示意图:
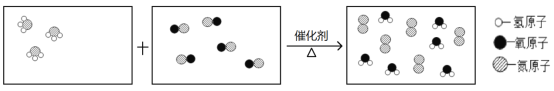
①请在左边两个方框内将反应过程的微观示意图补画完整_______
②请写出该反应的化学方程式___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列装置,回答问题:

(1)用高锰酸钾制取O2,装置A还需做的一点改动是_____。
(2)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过以下四步实验操作可回收二氧化锰。正确操作的先后顺序是_____(填写选项序号)。
a烘干 b溶解 c过滤 d洗涤
(3)把(2)中滤液蒸发结晶可得到氯化钾晶体,在蒸发操作中玻璃棒的作用是 ____。
(4)用装置F制取气体,在反应过程中,用弹簧夹夹住导气管上的橡皮管,过一会儿反应就会停止,其原因是 _____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年12月30日,我国首条智能化高速铁路“京张高速铁路”正式通车运营,这标志着中国首条“智能化”高速铁路的建设进入新阶段。
(1)铝合金被广泛应用于制造飞机、高铁等,因为铝合金具有_______(写一点即可)、密度小等特性。
(2)钪(Sc)合金是比铝合金更轻的合金。相同条件下,取金属钪和锌分别与相同浓度的盐酸反应,钪表面产生气泡的速率明显更快。根据上述现象,判断下列说法正确的是______(填序号)。
a. 将Sc投入CuSO4溶液中有红色物质析出
b.用Fe(NO3)2溶液、Sc(NO3)3溶液、Zn能验证钪和铁的活动性强弱
c.用Fe、Sc、稀H2SO4溶液能验证钪和铁的活动性强弱
(3)铁是目前世界上年产量最高的金属,请写出工业上用CO与赤铁矿反应冶炼铁的化学方程式________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定:在NaCl存在下,Na2S2O4在水中溶解度显著下降。Na2S2O4制备流程如图:
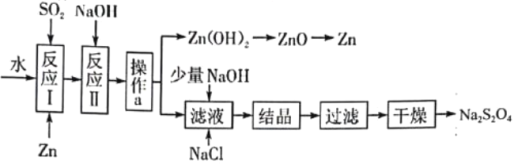
(1)反应I的原理为![]() ,该反应的基本反应类型为______。
,该反应的基本反应类型为______。
(2)反应II为复分解反应,该反应的化学方程式为______。
(3)氢氧化锌在加热的条件下分解生成两种氧化物,发生反应的化学方程式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com