
【题目】请你结合下列装置图回答问题:
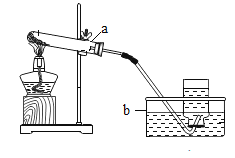
(1)写出标号仪器的名称:a、_____,b_____。
(2)实验室用加热氯酸钾和少量二氧化锰的方法来制取氧气,该反应的化学方程式是_____,基本反应类型是_____;实验结束后,将剩余的固体倒入烧杯中,加入足量的水,搅拌、_____,得到一种黑色粉末。该黑色粉末与过氧化氢接触,有大量气泡产生,黑色粉末在该反应中的作用是_____,反应的化学方程式是_____。
科目:初中化学 来源: 题型:
【题目】某同学用如图总结NaOH的四类化学性质(即NaOH能够与四类物质发生化学反应)。
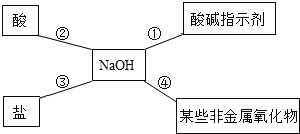
(1)为验证性质①,该同学将无色酚酞试液滴入NaOH溶液中,溶液颜色由无色变成_______________。
(2)性质②的反应为______________反应(非基本反应类型),试写出NaOH与盐酸反应的化学方程式_______________。
(3)为了验证性质③,该同学可选择的物质是_______________(填序号)
A Na2CO3 B CO2 C FeCl3 D Ba (NO3) 2
(4)写出NaOH溶液吸收CO2的化学方程式_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组用以下装置探究炼铁原理,关于该装置和反应过程描述错误的是( )
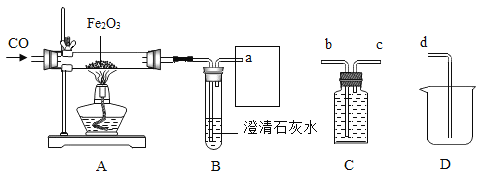
A. 盛装药品前应先检查装置气密性
B. 加热前要先通CO,加热后B中出现浑浊
C. 已知方框中连接的是C和D,导管口的连接顺序为a→b→c→d
D. 这种方法“炼”出的铁与工业上炼出的生铁在组成上最大的区别是不含碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“嗅盐”,又名“鹿角酒”,在某些体育运动场合被使用,比如拳击、举重等。当运动员陷入意识迷糊状态时,医生用嗅盐把运动员唤醒,以继续比赛。某校兴趣小组在老师的指导下,对“嗅盐”展开了系列探究:
(查阅资料)①嗅盐,主要成分是碳酸铵,给人闻后有恢复和刺激作用;
②嗅闻原理是碳酸铵晶体产生的氨气对人体有刺激作用,过量嗅闻不利健康;
③碳酸铵[(NH4)2CO3]晶体受热易分解,产生三种气体。
(定性初探)验证“嗅盐”的化学性质
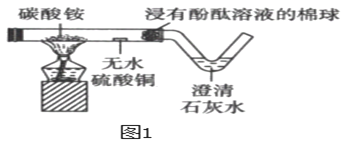
(1)某同学为验证碳酸铵晶体受热分解产生的三种气体设计了如下的实验装置(见图1)。
①无水硫酸铜变蓝说明有水蒸气生成;浸有酚酞溶液的棉球_____(填实验现象)说明有NH3产生;澄清石灰水变浑浊,说明有_____产生。
②根据实验写出碳酸铵受热分解的化学方程式_____。
(定量再探)测定“嗅盐”中碳酸铵(NH4)2CO3的质量分数
方案Ⅰ:取样品6.0克,用图2装置进行实验,测量C装置在反应前后增加的质量即为产生NH3的质量。(碱石灰的主要成分是氢氧化钠和生石灰)
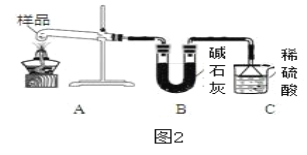
(2)装置B的作用是_____,装置C中倒置漏斗的作用是充分吸收气体并_____。
(3)小组同学经过讨论后,均认为用该套装置测量会导致碳酸铵的质量分数偏小,原因是_____。
方案Ⅱ:取样品6.0克,用图3装置进行实验,利用G装置测量反应生成气体的体积。(CO2几乎不溶于饱和的NaHCO3溶液)
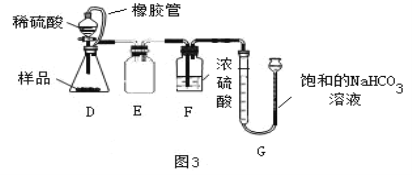
(4)请写出装置D中发生反应的化学方程式:_____。
(5)实验测得量气管中产生气体的体积为558mL,该方案所测嗅盐中碳酸铵的质量分数为。_____(已知实验条件下,CO2的密度约为1.97g/L)(请写出过程,计算结果精确到1%)
(6)若其他操作均正确,下列因素会导致所测嗅盐中碳酸铵的质量分数偏大的是_____
a、用水来代替饱和的NaHCO3溶液
b、实验结束后,调节两端液面相平读数
c、反应结束后未等装置冷却到室温,就开始读数
d、缺少橡胶管
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列曲线示意图不正确的是()
A.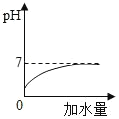 向稀盐酸中加蒸馏水(图中 q 曲线未与虚线相交,只无限接近)
向稀盐酸中加蒸馏水(图中 q 曲线未与虚线相交,只无限接近)
B. 等体积、等质量分数的过氧化氢分解
等体积、等质量分数的过氧化氢分解
C.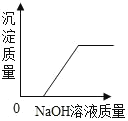 HCl 和 FeCl3的混合液中加入 NaOH 溶液
HCl 和 FeCl3的混合液中加入 NaOH 溶液
D.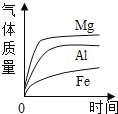 等质量、等颗粒大小的金属加入足量稀盐酸
等质量、等颗粒大小的金属加入足量稀盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】符合事实且化学方程式书写正确的是( )
A.用硝酸银溶液鉴别稀盐酸和稀硫酸:AgNO3+HCl═AgCl↓+HNO3
B.铁与盐酸反应制取氢气:2Fe+6HCl═2FeCl3+3H2↑
C.正常雨水 pH 值约为 5.6 的原因:CO2+H2O═H2CO3
D.点燃法除去 CO2 中混有少量的 CO:2CO+O2![]() 2CO2
2CO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】加热氯酸钾和二氧化锰的混合物可以制备氧气,该反应的化学方程式为____________,但实验中发现有刺激性气味的气体产生。请你一起参与探究:
(提出问题)刺激性气味的气体是什么呢?
(猜想假设)
猜想一:臭氧(化学式为O3)。
猜想二:HCl。
猜想三:Cl2
同学们认为猜想二不需要实验验证就可以判断是错误的,理由是____________。
(链接资料)
(1)Cl2 + H2O = HClO + HCl,HClO 在水溶液中可解离出少量H+、Cl、ClO;HClO 具有强氧化性和漂白性,可杀灭细菌病毒,使有色物质褪色;AgNO3 + HCl = AgCl ↓+ HNO3,AgCl 是一种白色沉淀。
(2)臭氧在二氧化锰存在情况下极易分解产生氧气。
(实验探究)
查阅资料后大家认为猜想一是错误的,理由为________。
他们进一步做了如下实验:取氯酸钾和二氧化锰的混合物放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管口,看到的现象是____________,再将湿润的蓝色石蕊试纸悬于试管口,试纸____________最终证明猜想三正确。
(反思拓展)
自来水厂常用漂白粉杀菌消毒[主要成分化学式为 Ca(ClO)2在水中起杀菌消毒作用的离子是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com