
【题目】以1-18号元素为研究对象,请回答下列问题:
(1)l~18号元素中最外层有2个电子的原子有______、Be、Mg(填元素符号)。
(2)氮化钠是科学家制备的一种重要的化合物,在室温时为晶体,在低于室温时会变成非晶体,高于87℃时会分解为钠单质及氮气,氮化钠的化学式是___________。
(3)某粒子的结构示意图为 (y≠0),当x-y=8时该粒子的符号为________。
(y≠0),当x-y=8时该粒子的符号为________。
(4)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。与N2O互为等电子体的粒子符号为_________。
【答案】He Na3N S2- CO2
【解析】
利用l~18号元素的结构示意图以及化合价与最外层电子数的关系解答。
(1) 根据l~18号元素的核外电子排布的规律知,最外层有2个电子的原子有:2号元素He,4号元素Be,12号元素Mg,故填:He;
(2)氮元素的质子数为7,根据核外电子排布规律,其原子最外层电子数为5,易得3个电子,形成8个电子的稳定结构,所以氮元素的化合价可显-3价,而金属钠通常显+1价,则氮化钠的化学式为Na3N,故填:Na3N;
(3)根据原子结构的特征:在原子中,质子数=核外电子总数,从结构示意图可知在原子中的等量关系:x=10+y,而此题的信息是x-y=8,即x=8+y,说明此粒子结构示意图为离子结构示意图,而在离子结构示意图中最外层是8个电子的稳定结构,所以y=8,代入等式知x=16,核外电子数为18个,质子数为16的元素是硫元素,所以此粒子是硫离子,符号为S2-,故填:S2-;
(4)具有相同原子数和电子数的分子或离子叫等电子体。N2O的原子数为3,电子数为22,而CO2的原子数为3,电子数为22,所以CO2与N2O互为等电子体。故填:CO2。


科目:初中化学 来源: 题型:
【题目】松油醇(C10H18O)是一种调香香精,多存在于松节油、芳樟油、玉树油、橙花油中,请回答:
(1) 松油醇的相对分子质量是______________________;
(2) 松油醇中碳元素、氢元素、氧元素的质量比是____________________;
(3)15.4 g松油醇所含碳元素质量与_______________________ g葡萄糖(C6H12O6)所含碳元素质量相等。(要有计算过程,精确到0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列实验装置图,回答有关问题。

(1)图甲是实验室加热高锰酸钾制取氧气的发生装置,实验时应在试管口塞一团棉花,其作用是_____。试管中发生反应的符号表达式为_____,属于_____反应(反应类型)。
(2)图乙中标号仪器①的名称_____。
利用图乙进行下列实验:
I:开始先关闭K2,打开K1,片刻后观察到烧杯中蜡烛燃烧更剧烈,A中发生反应的符号表达式为_____,其中二氧化锰的作用是_____。
Ⅱ:然后关闭K1,打开K2,观察到烧杯中蜡烛燃烧不旺直至熄灭,B中发生反应的符号表达式为_____,蜡烛逐渐熄灭说明二氧化碳具有的化学性质是_____。
气体 | 药品 | 条件 |
①氢气 | 锌粒和稀硫酸 | 常温 |
②氯气 | 二氧化锰和浓盐酸 | 加热 |
③硫化氢 | 硫化亚铁固体和稀硫酸 | 常温 |
(3)下列三种气体能选用图乙中A作为发生装置的是_____(填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线。

下列说法正确的是
A. 在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V时所得溶液的pH越大
B. 在a曲线所示的实验中,若用酚酞做指示剂,酚酞溶液由红色变为无色
C. 在a、b、c三种曲线所示的实验中,反应速率相同
D. 在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~I均为初中化学常见物质,它们之间的转化关系如下图,部分产物已略去。
已知A是人体胃酸的主要成分,B是大理石的主要成分,D为液体,F为气体,I能与A反应生成个数比为1: 2的+2价、+3价铁盐。
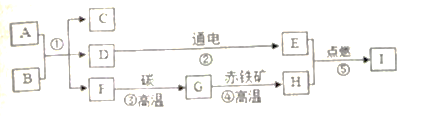
(1)写出下列物质的化学式:C______;
(2)上述①②③④⑤中属于化合反应的是______;
(3)写出G→H的化学反应方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:Cu与稀硫酸(H2SO4)不反应,Zn+H2SO4===ZnSO4+H2↑。某同学将20g黄铜(铜和锌的混合物)放入烧杯中,向烧杯中滴加稀硫酸至过量,实验测得加入稀硫酸的质量与产生氢气质量的关系如下图所示。请计算:

(1)恰好完全反应时生成氢气的质量是_____g;
(2)该黄铜中锌的质量分数是多少?___________
(3)若恰好完全反应时加入稀硫酸的质量为100g,则恰好完全反应时烧杯内物质的质量为______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)甲、乙是常见元素的单质,A、B是常见的化合物,它们的反应表达式是甲+A=B+乙(式中各物质的化学计量数和反应条件已略去)。请回答:
①该反应的类型是_______________。
②若甲、乙为金属,且甲的化合物溶液为蓝色,写出反应的化学方程式____________________________。
③若乙为非金属单质,B中含有+3价金属元素,写出反应的化学方程式____________________________。
(2)如图所示。常温下,某无色液体X中加入一种固体Y,观察到气球涨大。猜测可能情况。
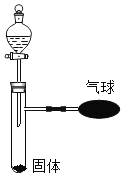
无色液体X的名称 | 固体Y的名称 | 反应的化学方程式 | |
__________ | __________ | _______ | |
__________ | __________ | ________ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法不正确的是( )
物质 | X | Y | Z | W |
反应前质量/g | 10 | 3 | 90 | 0 |
反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
A. W可能是单质 B. Y可能是催化剂
C. 该反应是分解反应 D. 反应后Z物质的质量为![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合如图所示实验,回答问题。
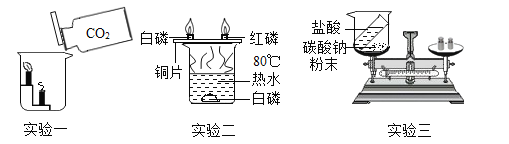
![]() 由实验一可知,
由实验一可知,![]() 具有的物理性质是______;
具有的物理性质是______;
![]() 在实验二中,铜片上的白磷燃烧,水中的白磷不燃烧,由此能够得出燃烧的条件之一是______。
在实验二中,铜片上的白磷燃烧,水中的白磷不燃烧,由此能够得出燃烧的条件之一是______。
![]() 在实验三中,通过测定盐酸和碳酸钠粉末反应前后的质量来验证质量守恒定律,前后两次称量结果不一致,原因是______。
在实验三中,通过测定盐酸和碳酸钠粉末反应前后的质量来验证质量守恒定律,前后两次称量结果不一致,原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com