
【题目】某学校几个兴趣实验小组利用石灰石(杂质不参与反应也不溶于水)制备轻质CaCO3并研究CaSO42H2O加热分解的产物。
(一)轻质碳酸钙的制备

已知:Ca(OH)2、NaOH和Na2CO3都显碱性,溶液可以使无色酚酞变红色。
(1)副产品氢氧化钠俗称____________(写一个即可)。
(2)该流程方案中有两个反应,产物中均出现碳酸钙,这两个反应的化学方程式分别为
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH和______________________。
(3)为验证加入Na2CO3溶液后,溶液M中的溶质是否反应完全,可取上层清液加入____(填字母)进行检验。
A碳酸钠溶液 B铁粉 C无色酚酞试液
(二)研究CaSO42H2O加热分解的产物。
利用(一)中轻质碳酸钙粉末与硫酸反应,经过一系列操作可以分离得到CaSO42H2O样品。已知:分离所得的CaSO42H2O样品中含有的CaCO3,可用盐酸除去。
(4)为了测定样品中CaSO42H2O的含量。某实验小组取10g该样品,加入足量的稀盐酸,充分反应后,产生气体的质量为0.44g,则该样品中CaSO42H2O的质量分数为________。[写出具体解题过程]
(5)为测定CaSO42H2O和CaCO3的质量比x:y,某实验小组利用如图2所示的装置(夹持仪器省略)进行实验。
查阅资料:a.CaSO42H2O在160℃生成CaSO4,1350℃时CaSO4开始分解;CaCO3在900℃时分解完全。b.碱石灰的主要成分是NaOH和CaO的混合物。
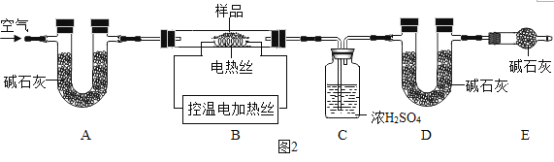
①实验前首先要_______________,再装入样品;
②装置A的作用是_____________;装置E的作用是_____________。
③现控制B装置温度900℃进行实验并采集了如下数据:a.装置C实验后增重m1g b.装置D实验后增重m2g。某同学利用采集的数据求出x:y的值,若无装置E,则实验测定结果将_______(填“偏大”、“偏小”或“无影响”)
(6)已知CaSO42H2O受热会逐步失去结晶水。取纯净CaSO42H2O(相对分子质量为172)固体3.44g,放在(5)的实验装置B中进行加热,测定固体质量随温度的变化情况如图3所示。
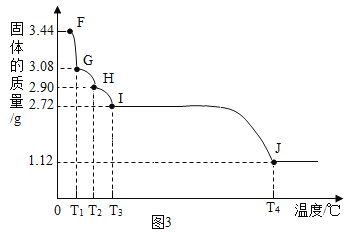
①G点固体的化学式是____________;
②在T3~T4℃温度段加热固体产生两种气体,其中一种气体有刺激性气味,则I~J段发生反应的化学方程式为____________________。
【答案】烧碱、火碱、苛性钠(写一个即可) Ca(OH)2+CO2=CaCO3↓+H2O A 90% 检查装置的气密性 除去空气中的CO2和H2O 防止空气中的CO2和H2O进入D 偏小 CaSO4H2O 2CaSO4![]() 2CaO+2SO2↑+O2↑
2CaO+2SO2↑+O2↑
【解析】
(1)氢氧化钠俗称烧碱、火碱、苛性钠;
(2)石灰石高温煅烧生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(3)碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,所以溶液M中的溶质是否反应完全,可取上层清液加入碳酸钠溶液进行检验;
(4)设参加反应的碳酸钙的质量为x,
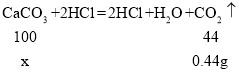
![]()
x=1g;
所以该样品中CaSO42H2O的质量分数为![]() ×100%=90%;
×100%=90%;
(5)①有气体参加的反应,实验前首先要检查装置的气密性,再装入样品;
②装置A的作用是除去空气中的CO2和H2O,防止它们影响实验结果,装置E是为了防止空气中的二氧化碳和水蒸气进入装置D,影响实验结果;
③装置E的作用是吸收空气中的水和二氧化碳,如没有装置E,则实验测定结果将偏小;
(6)①设G点固体的化学式为CaSO4xH2O,则:
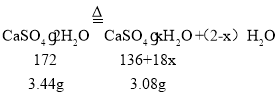
![]()
x=1;所以G点固体的化学式是CaSO4H2O;
②将T2~1400℃温度段加热产生两种气体,其中一种气体有刺激性气味,说明生成了二氧化硫气体,所以H~I段发生反应的化学方程式为:2CaSO4![]() 2CaO+2SO2↑+O2↑。
2CaO+2SO2↑+O2↑。


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为了研究蜡烛燃烧的产物,设计了以下实验,如图所示。取A、B两个空集气瓶,瓶底分别装有澄清石灰水和无水硫酸铜,瓶口均用玻璃片盖好。(已知:无水硫酸铜为白色固体,遇水会变成蓝色)
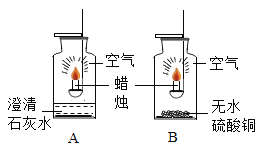
①点燃集气瓶A中的蜡烛,观察到蜡烛燃烧的产物使澄清石灰水变浑浊;
②点燃集气瓶B中的蜡烛,发现蜡烛燃烧的产物使无水硫酸铜变成蓝色。
请回答:
(1)蜡烛在氧气中燃烧的过程是________(填字母)。
A 物理变化 B 化学变化 C 既有物理变化又有化学变化
(2)以上实验说明蜡烛的燃烧产物有:_________、_________。
(3)蜡烛燃烧时,火焰分为三层,由外而内依次为__________、__________、_______,其中__________温度最高。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是一种打火机的示意图。请根据有关信 息回答下列问题:
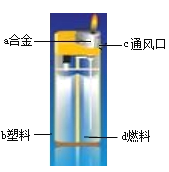
(1)构成打火机的材料中属于合成材料的是________(填标号)。
(2)其燃料的主要成分丁烷(C4H10)属于________(填“有机”或“无机”)化合物,丁烷在通常状况下呈气态,请用分子的基本性质解释丁烷气体能被压缩成液体的原因__________________。
(3)打火机挡风罩通风孔的作用是使空气流通,说明燃料燃烧必须与____________接触。若通风孔通气不良,可能造成打火机无法起火或燃料不完全燃烧而生成_____________有毒气体,既浪费了燃料又污染了环境。用打火机点火是利用燃料燃烧将化学能转化为_____________能。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图为甲、乙两种固体物质(不考虑结晶水) 的溶解度曲线。下列说法错误的是
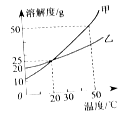
A.20 ℃时,甲、乙具有相同的溶解度
B.甲、乙的溶解度都随温度的升高而增大
C.20 ℃时,可以配制溶质的质量分数为25%的甲溶液
D.50℃时,甲和乙各30g分别加入100g水中,充分溶解后同时等速降温,则乙溶液中先有固体出现
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】稀土元素在科技生产中有广泛的用途,被誉为新材料的宝库。如图为稀土元素镱在元素周期表中的信息,下列说法正确的是

A. 镱元素是非金属元素
B. 一个镱原子的核内中子数为70
C. 一个镱原子的核外电子数为70
D. 镱元素的相对原子质量为173.0g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是铁丝在氧气中燃烧的实验。请回答:
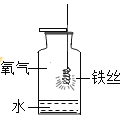
(1)反应的实验现象是________________ ;
(2)反应的化学方程式为___________ ;
(3)集气瓶中加入少量水的作用是_______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请仔细分析下列化学反应,回答下列问题:
①2H2+O2![]() 2H2O;②2CO+O2
2H2O;②2CO+O2![]() 2CO2;③ 3Fe+2O2
2CO2;③ 3Fe+2O2![]() Fe3O4
Fe3O4
(1)反应①~③有许多共同点。如:它们的生成物都属于____________。请你再指出它们的一个共同点:____________;
(2)反应①~③也有许多不同之处,请仿照示例指出其中一点(答案不能与示例相同)。示例:③的方程式中化学计量数之比为3︰2︰1,而另两个是2︰1︰2。不同之处:_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚进行了相关探究.

【查阅资料】这种“白色粉末”的主要成分是过碳酸钠(化学式为Na2CO4),常温下,与水反应生成氧气.【实验1】小明选用如图所示装置中的 (选填序号)进行过碳酸钠与水的反应并收集产生的气体,经检验该气体是氧气,检验方法是
【提出问题】过碳酸钠与水反应后得到的溶液M中溶质的成分是什么?
【作出猜想】根据过碳酸钠与水的组成作出三种猜想.
猜想一:Na2CO3;猜想二:NaOH;猜想三:Na2CO3和NaOH.
【实验2】小明取溶液M,滴加CaCl2溶液,观察到有白色沉淀生成,他认为白色沉淀是CaCO3,溶液中一定含有Na2CO3.小刚提出质疑,产生的白色沉淀不一定是CaCO3,他的理由是: .
【实验3】小刚取溶液M,滴加稀HCl,观察到 ,证明溶液中一定含有Na2CO3,从而否定了猜想二.Na2CO3与稀HCl反应的化学方程式为 .
【实验4】为进一步确定溶液M中是否含有NaOH,他们向溶质M中滴加CaCl2溶液至不再产生沉淀为止,取上层溶液,加入 ,无明显现象.证明溶液中无NaOH溶液,猜想一正确.该实验中用CaCl2溶液而不用饱和石灰水,原因是: .
【反思拓展】
(1)根据过碳酸钠的性质,保存时应注意防潮.
(2)检验A、B两种物质是否同时存在,一定要考虑二者性质的互相干扰问题.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图回答问题。
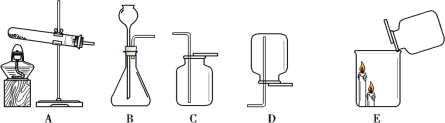
(1)实验室用高锰酸钾制取氧气时,选用的收集装置是_______(填字母序号,下同)。发生反应的化学方程式为_______。
(2)实验室用大理石和稀盐酸制取二氧化碳的化学反应方程式为_____,选用的发生装置是_____。
(3)如图E所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com