

| 实验操作 | 实验现象 | 实验结论 |
| 取少量工业烧碱样品配成溶液后,滴加过量 |
工业烧碱中含有碳酸钠,产生实验现象的化学方程式: |


 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:初中化学 来源: 题型:
 每逢中秋,家人团聚,餐桌上少不了哈尔滨的特产“老鼎丰”月饼,食用后能为人体补充的营养素主要是
每逢中秋,家人团聚,餐桌上少不了哈尔滨的特产“老鼎丰”月饼,食用后能为人体补充的营养素主要是查看答案和解析>>
科目:初中化学 来源: 题型:
| A、稀释浓硫酸时,一定要将水慢慢注入浓硫酸中,并不断搅拌 |
| B、实验室制取气体时,应先检验装置的气密性 |
| C、为了达到节约药品的目的,将实验后剩余的药品放回原瓶 |
| D、测定溶液的pH值,应先用水润湿pH试纸 |
查看答案和解析>>
科目:初中化学 来源: 题型:
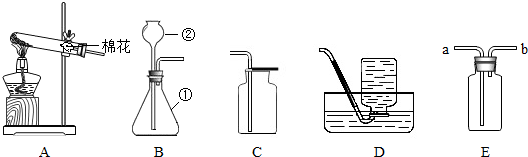
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
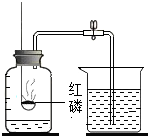
| 1 |
| 5 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com