
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1~6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变成黑色 |
| 实验操作 | 实验现象 |
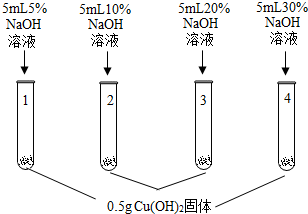 | 1号试管,… 2号试管,蓝色固体不消失 3号试管,蓝色固体减少 4号试管,蓝色固体消失,得到亮蓝色溶液 |
分析 根据硫酸铜和氢氧化钠反应产生氢氧化铜蓝色沉淀和硫酸钠,写出反应的方程式;
【猜想与假设】根据实验①的现象是沉淀消失,形成亮蓝色溶液,而不是产生黑色固体分析;
【解释与结论】(1)根据随着氢氧化钠溶液的浓度增大而氢氧化铜不断溶解进行解答;
(2)根据实验现象分析得出实验结论进行解答;
【反思与评价】(1)根据信息结合方程式的书写写出反应的方程式;
(2)根据现象及资料信息分析能量变化.
解答 解:硫酸铜和氢氧化钠反应产生氢氧化铜蓝色沉淀和硫酸钠,故反应的方程式为:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
【猜想与假设】根据实验①的现象是沉淀消失,形成亮蓝色溶液,而不是产生黑色固体,因此猜想Ⅰ认为蓝色沉淀消失可能是Cu(OH)2发生了分解是错误的;
【解释与结论】(1)随着氢氧化钠溶液的浓度增大而氢氧化铜不断溶解,所以1号试管中现象为:蓝色固体不消失;
(2)由实验现象可知,氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液;
【反思与评价】(1)氢氧化铜在氢氧化钠溶液中溶解生成铜酸钠,反应的化学方程式为2NaOH+Cu(OH)2=Na2Cu(OH)4;
(2)Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,因此说明饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应.
故答案为:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
【猜想与假设】氢氧化铜分解生成黑色的氧化铜固体;
【解释与结论】(1)蓝色固体不消失;
(2)氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液;
【结论与反思】(1)2NaOH+Cu(OH)2=Na2Cu(OH)4;
(2)蓝色沉淀逐渐变为黑色.
点评 本题属于信息题的考查,解题的依据是题目的信息结合已有的相关知识进行分析,能够考查学生的知识迁移能力.


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:初中化学 来源: 题型:解答题
 用科学方法认识和改造物质
用科学方法认识和改造物质查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
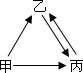 甲、乙、丙之间有如图所示的转化关系(部分物质和反应条件已经略去).
甲、乙、丙之间有如图所示的转化关系(部分物质和反应条件已经略去).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com