
分析 红磷燃烧生成五氧化二磷;
氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,从而可以除去氯化钠中的碳酸钠;
甲醇燃烧生成水和二氧化碳;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:(1)红磷燃烧的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)氯化钡和碳酸钠反应的化学方程式为:BaCl2+Na2CO3═BaCO3↓+2NaCl;
(3)甲醇燃烧的化学方程式为:2CH3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O;
(4)硝酸银分解的化学方程式为:2AgNO3$\frac{\underline{\;光\;}}{\;}$2Ag+2NO2↑+O2↑.
故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;BaCl2+Na2CO3═BaCO3↓+2NaCl;2CH3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O;2AgNO3$\frac{\underline{\;光\;}}{\;}$2Ag+2NO2↑+O2↑.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:初中化学 来源: 题型:解答题
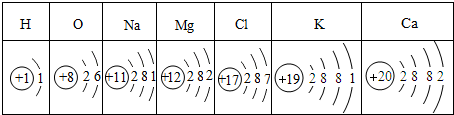
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
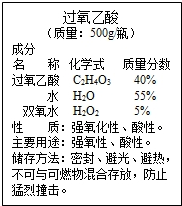 如图为某过氧乙酸标签的部分文字说明,请回答:
如图为某过氧乙酸标签的部分文字说明,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 失去1 mol电子 | B. | 得到1 mol电子 | C. | 失去2 mol 电子 | D. | 没有电子得失 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
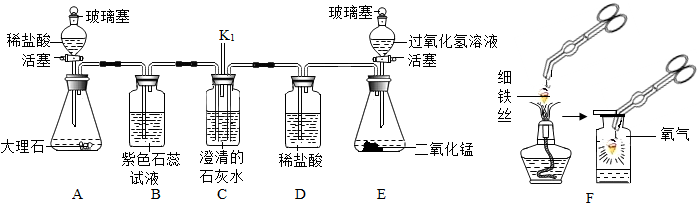
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com