
����Ŀ��̼�����һ�ֳ��õIJ��Ƽ����������оͺ���̼��ơ�Ϊ�ⶨ��������̼��Ƶĺ�������ѧ��ѧ������ѧ���úû�ѧ��ѧϰС���ͬѧ��ȡ20g������鼦���Ƿ����ձ��У��������м���80gϡ����ǡ����ȫ��Ӧ��ע�������в�����Ԫ�أ�Ҳ�������ᷴӦ��ʵ����̲����Ķ�����̼ȫ���ݳ�������Ӧ�����е�ͼ������ͼ��ʾ����ش�
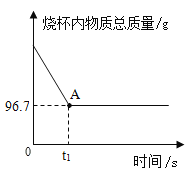
��1�����ڷ�Ӧ������˵��A���ʾ��_____��
��2��ʵ�����������CO2����_____g��
��3����20g�������к�̼��Ƶ���������Ҫ��д��������̣�____
��4����20g�������к���Ԫ�ص���������Ҫ��д��������̣�________
���𰸡��������е�̼���������ǡ����ȫ��Ӧ 3.3 7.5g 3g
��������
��1������A��ʱ���ձ������ʵ����������ڼ��ٷ�����
��2�����������غ㶨�ɷ�����
��3�����ݷ�Ӧ�Ļ�ѧ����ʽ���ɷų�������̼���������㵰��������̼��Ƶ�������
��4�����ݻ�������ijԪ�ص�����=�û��������������Ԫ�ص��������������з������
��1����ͼ��֪��A��ʱ���ձ������ʵ����������ڼ��٣�˵����Ӧǡ��ֹͣ������������е�̼���������ǡ����ȫ��Ӧ��
��2�����������غ㶨��ʵ����������ɶ�����̼������Ϊ�ձ������ʼ��ٵ���������20g+80g-96.7g=3.3g�����3.3��
��3���⣺�輦������̼��Ƶ�����Ϊx

![]() �����x=7.5g���ʴ�Ϊ��7.5g��
�����x=7.5g���ʴ�Ϊ��7.5g��
��4����Ԫ�ص�����Ϊ7.5g��![]() ��100%=3g���ʴ�Ϊ��3g��
��100%=3g���ʴ�Ϊ��3g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С�������ͼʾʵ��٢ڢۣ������ж���ȷ���ǣ�������

A.ʵ�����ʯ��ˮ��ʣ��
B.ʵ����������ݲ���
C.ʵ�����û����������
D.ʵ���������Һ��һ����CaCl2��NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɰHgS��֮��ˮ���������ֻ��ɵ�ɰ������������CuSO4Ϳ��������ɫ��ͭ����������������д��������![]() ������
������![]() �������й�˵������ȷ����
�������й�˵������ȷ����
A.����ɰHgS��֮��ˮ����ˮ��ָ���ǵ��ʹ���������ΪҺ̬
B.��������CuSO4Ϳ��������ɫ��ͭ�������Ļ�ѧ��ӦΪ![]()
C.�����������漰�����ֵ��ʣ�������ѧ��Ӧ
D.�����������漰�Ļ�ѧ��Ӧȫ�������û���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼʾ��A��E�dz��л�ѧ���������ʡ���������ᡢ��η��࣬A��B��C��D�����ֲ�ͬ�������ʣ�E�Ǵ���ʯ����Ҫ�ɷ֡�ͼ����������ʾ��������������֮����Է�����Ӧ����������ʾijһ�����ʾ�һ����Ӧ��ת��Ϊ��һ�����ʡ������ַ�Ӧ������P��Ӧ��������ȥ������ش��������⣺

��1��E�Ļ�ѧʽΪ_____��
��2����Ӧ�ٵĻ�ѧ����ʽΪ_____��
��3������A�����Ϊ_____������������ᡢ�����һ�֣�
��4����Ӧ�ڵķ�Ӧ����_____������һ��������һ������������һ�������ǻ��Ϸ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ����ʹ�ú���ȼ�յķ����ⶨ�����������ĺ���������˵������ȷ����
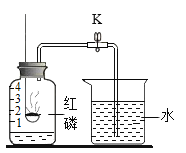
A.ȼ�յĺ���һϨ�𣬾�Ҫ�������ɼУ�����¼ˮ���뼯��ƿ�Ŀ̶�
B.ʹ�ú���������٣�������Ӱ��ʵ����
C.ȼ�������ĺ��ף���ʹ���뼯��ƿ��ˮռ����ƿ�����4/5
D.ȼ�յĺ���Ϩ���һ���������ƿ��ѹǿ�½�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ں����ʵ���۽����У���ȷ����( )
A. ��������̼�����Ƴɸɱ������С![]() ���������С
���������С
B. ������������ȼ������ˮ![]() ��ѧ��Ӧ�з��Ӻ�ԭ�Ӷ������ٷ�
��ѧ��Ӧ�з��Ӻ�ԭ�Ӷ������ٷ�
C. ��Ȼ����ˮ����Ȼѭ��![]() ˮ���Ӳ����˶��ҷ��Ӽ�ļ�������ı�
ˮ���Ӳ����˶��ҷ��Ӽ�ļ�������ı�
D. ʳ�����![]() ʳ���еķ�������䣬�����ӵ����ʷ����˱仯
ʳ���еķ�������䣬�����ӵ����ʷ����˱仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ��װ�ã��ش��й����⡣
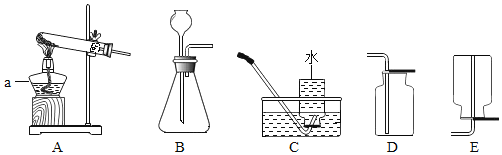
��1��д��ͼ������a�����ƣ�____��
��2��ʵ�����ü��ȸ�����ط�����ȡ������Ӧѡ��ķ���װ��Ϊ_������ĸ����ͬ����������Ӧ�Ļ�ѧ����ʽΪ____��
��3��ʵ������ʯ��ʯ��ϡ���ᷴӦ��ȡ������̼��Ӧѡ����ռ�װ��Ϊ__��
��ѧ���Դ˷�Ӧ�����Һ����Ȥ����ȡ������Ӧ����˵���ҺM����ε���̼������Һ��̼������Һ�Լ��ԣ�������pH������������⣬�õ���ͼ��ʾ������ͼ��������ΪpH��������Ϊʱ�䣩��
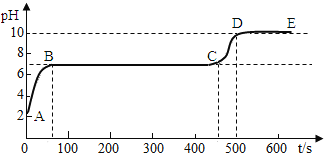
��.��������ͼ��ȷ����ҺM�ijɷ�____��д��ѧʽ������д��BC���ڷ����Ļ�ѧ��Ӧ����ʽ____��
��.ͼ��CD��������ԭ������Ϊ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС������ȥ�����Ȼ����л��������������Ȼ�þ����������ɳ�������ͼ��ʾʵ�鷽���������ʵ�鲢�ش����⡣

(1)���������������������_____��
(2)����ڡ����У�����X��������_____��
(3)������У������������������Һ��Ŀ����_____������B�Ļ�ѧʽ��_____��
(4)д����Ӧ�۷����Ļ�ѧ����ʽ��______
(5)��ͬѧ��Ϊԭʵ�鷽�������ƣ������������۵�������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��һ����Ȼ��ѧ�����������о����ʺʹ������ʡ�
��1������̫���ܵ�غ͵���оƬ����ȱ�ٵIJ��ϡ���������ʯӢɰ����Ҫ�ɷ��Ƕ������裩�Ƶøߴ��衣�����ߴ��������ʾ��ͼ����:
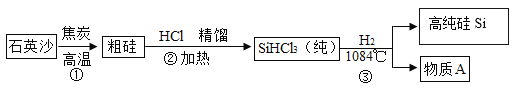
���Ʊ��ֹ�ķ�ӦΪ��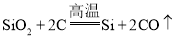 ���÷�Ӧ����___��Ӧ��ѡ�����ֽ��������������û��������ֽ���֮һ����
���÷�Ӧ����___��Ӧ��ѡ�����ֽ��������������û��������ֽ���֮һ����
���Ʊ��������õ�H2���ڵ�ȼ�����H2ǰ��Ӧ���Ƚ��еİ�ȫ������_____��
������Aͨ��״����Ϊ��ɫ�д̼�����ζ�����壬����ˮ�γ�һ�ֳ������ᣬд��������еĻ�ѧ��Ӧ����ʽ_______��
��2��������������ҡ������ˮ�����DZ����ˮ��Դ�������̲��ŷḻ�Ļ�ѧ��Դ����ǿ�Ժ�ˮ��Դ�Ŀ������ã��ǽ���ҹ��غ�����������ˮ������ˮΣ������Դ��ȱ�������Ҫ��ʩ����ʵ�ֹ��ÿɳ�����չս�Ե���Ҫ��֤���Ӻ�ˮ��ȡ�õ�ˮ�Ĺ��̳�Ϊ����ˮ���������������õĺ�ˮ����������Ҫ��Ϊ�����ȷ�����Ĥ�������ࡣ
��ͼ��ʾ���Ե���Ĥ�Ҳ�ĺ�ˮ��ѹ��ˮ���ӿ���������Ĥ������൭ˮ�أ�����ˮ����Щ�������Ӳ���ͨ������Ĥ���Ӷ��õ���ˮ��
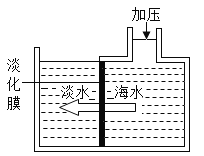
�ٽ�������ѹ����Ҳຣˮ���ڱ������У��þƾ��Ƽ��ȣ�ˮ�����ɺ��ڱ������Ϲ۲쵽��������_______��
�����жԼ�ѹ���Ҳຣˮ�ɷֱ仯����ķ����У���ȷ����___����ѡ���
A ������������
B �ܼ���������
C ��Һ��������
D ��������������С
�۰���ƴ�������ͨ����ѧ��Ӧ����NaHCO3��NH4C1��NaHCO3�ᾧ�������ټ���NaHCO3���Ƶô������NaHCO3��NH4C1���ܽ�����ش��������⣺
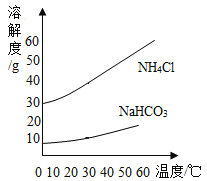
a.40��ʱ��NH4Cl������Һ��������������_____NaHCO3������Һ����������������ѡ������������С������������֮һ����
b.��30��ʱNH4Cl�ı�����Һ���µ�50���������Һ�Ǵ��¶���NH4Cl����Һ___��ѡ����������������������֮һ��
c.20��ʱ����30 gNaHCO3��������100gˮ�У��γɵ���Һ�Ǵ��¶���NaHCO3��____��Һ��ѡ����������������������֮һ����
d.��50��ʱ����������NaHCO3��NH4Cl������Һͬʱ���µ�20�棬_____�������������϶ࣨ�ѧʽ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com