
【题目】下图是KNO3和NaCl的溶解度曲线。

(1)20℃时,在100g水中加入40gNaCl固体,所形成的溶液是_______(填“饱和”或“不饱和”)溶液。
(2)50℃时,KNO3溶液的质量分数最大值是____________(只列计算式)。
(3)将50℃KNO3的饱和溶液降温到20℃,其溶液质量分数_______(填“变大”或“变小”或“不变”)。
(4)欲从NaCl溶液中获得大量的NaCl晶体,采用的方法是___________________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:初中化学 来源: 题型:
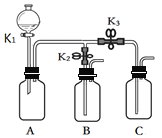
【题目】化学小组的同学用下图所示装置进行如下实验,实验前K1、K2、K3均为关闭状态。
内容 步骤 | 实验步骤 |
实验1 | B、C中分别盛有无色酚酞试液,打开K1,从分液漏斗中加入浓氨水,关闭K1,然后打开K2、K3。 |
实验2 | A中盛满CO2,B中盛有氢氧化钙溶液,C中盛有稀盐酸。 ①打开K1,从分液漏斗慢慢放入适量的氢氧化钠溶液,关闭K1。 ②一段时间后打开K2,观察到有A中有沉淀产生时,迅速关闭K2。 ③再打开K3,观察到A中有气泡产生。 |
(1)实验1中,可以观察到的现象是__________。
(2)实验2中,步骤①中所发生反应的化学方程式为____________________。
(3)实验2中,请解释步骤③产生气泡的原因为____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】市售加碘盐是在食盐中加入一定量的碘酸钾(KIO3)。请按要求进行计算:
(1)碘酸钾中钾元素、碘元素、氧元素的原子个数比为___________。
(2)碘酸钾中钾元素、碘元素、氧元素的质量比为___________。
(3)求碘酸钾中碘元素的质量分数_____________。(计算结果保留至0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)暖水瓶内胆玻璃上镀有一层银,某活动小组利用废弃的暖水瓶内胆设计如图所示实验(其中分离混合物的操作已略去)。

资料:Ag+2HNO3(浓)=AgNO3+NO2↑+H2O 3Ag+4HNO3(稀)=3AgNO3+NO↑+2H2O
⑴根据资料,不考虑反应速率的差异,实验时选用浓硝酸还是稀硝酸?说明理由。
⑵滤渣成分可能存在多种情况,推断其中成分最简单的滤渣对应的滤液中溶质的组成。
⑶设计实验对成分最复杂的滤渣进行验证,填写实验报告。
滤渣成分 | 实验操作及现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型多功能水处理剂。下图为制取(K2FeO4)的流程,请根据图示回答下列问题:

(1)固体B中含有的物质是_______________________;
(2)操作I的名称是_________,玻璃棒在操作中的作用是____________;
(3)请写出反应①的化学方程式________;反应②属于______反应(填基本反应类型);
(4)写出溶液C中溶质的一种用途_________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近几年来,全国各地掀起苹果醋饮料风,苹果酸(C4H6O5)是苹果醋的主要成分之一,下列说法错误的是
A. 苹果酸中碳、氢、氧三种元素的质量比为 4:6:5
B. 苹果酸由碳、氢、氧三种元素组成
C. 苹果酸的相对分子质量为 134
D. 苹果酸中氧元素的质量分数为60%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示(mol·L-1是浓度的一种表示方法)。下列说法正确的是
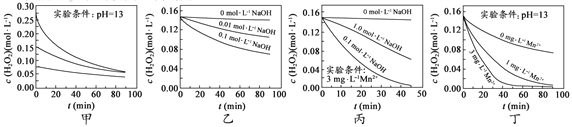
A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液pH越大,H2O2分解速率越快
C. 图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丁表明,碱性溶液中,Mn2+浓度越大,H2O2分解速率越快
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)如图1是元素周期表中的一部分,图2是铜原子的结构示意图。据图回答:
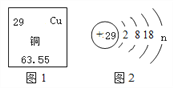
①图2中n的值为____;铜元素位于元素周期表中的第____周期。
②古代青铜器工艺精湛,但出土的青铜器表面大都锈蚀,锈蚀部分存在CuCl,CuCl的化学名称为________,为防止出土的青铜器再锈蚀,文物工作者将糊状Ag2O涂在被腐蚀部位,Ag2O与CuCl发生复分解反应,可以防止青铜器进一步被腐蚀,写出该反应的化学方程式_______。某新出土的青铜器通过分析测得Sn、Pb的质量分别为119 g、20.7 g,则该青铜器中Sn和Pb原子的数目之比为__。
(2)二氧化氯(ClO2)是一种高效净水剂。以粗盐为原料生产ClO2的工艺主要包括:A. 粗盐精制;B. 特殊条件下电解NaCl溶液制NaClO3;C. ClO2的制取。工艺流程如图。
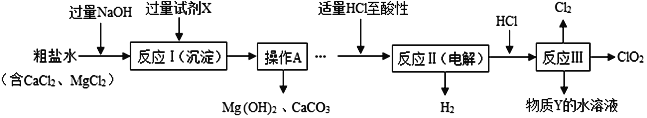 (其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl==2ClO2↑+Cl2↑+2NaCl+2H2O)
(其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl==2ClO2↑+Cl2↑+2NaCl+2H2O)
①试剂X中溶质的化学式为________________;操作A名称_____________。
②分析完成反应Ⅱ的化学方程式:_______________________________。
③我国最近已研究出ClO2的新制法,其反应的微观过程如图所示:
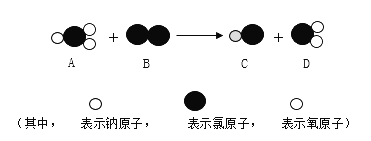
该反应的化学方程式是___________________;该反应中,反应物和生成物所属物质类别有________类。
(3)下图中A~H是初中化学常见的物质。B是最常用的溶剂,E有很好的抗腐蚀性能;D、E、F、H是四种不同类别的物质,且均含有地壳中含量最高的金属元素;四个虚线圈中的反应各属于四个不同的基本反应类型。图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
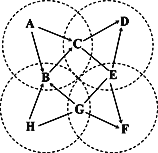
①写出H的化学式:___________。
②写出相关的反应的化学方程式:A→C:_____________; E—G:______________。
③G中一定含有(填元素符号)_______元素。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的转化关系如右图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列选项不能实现图示转化的是
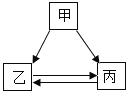
选项 | 甲 | 乙 | 丙 |
A | H2SO4 | H2 | H2O |
B | C | CO | CO2 |
C | Ca(OH)2 | CaCl2 | CaCO3 |
D | NaOH | NaCl | NaNO3 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com