在电子工业上,常用氯化铁溶液来腐蚀铜,制造电路板.据报道,通常状况下,铜与氯化铁溶液反应转化为氯化铜(氯化铜能溶于水).
(1)请完成该反应的化学方程式:Cu+2FeCl3═CuCl2+2______,该反应______(填“属于”或“不属于”)置换反应.
(2)若把一块铜板(足量)放入1000g溶质质量分数为16.25%的氯化铁溶液中,充分反应,待反应停止后取出铜片(假设无其它反应发生,操作过程中无损耗).
求:
①反应前溶液中溶质的质量.
②反应后所得溶液的质量.
解:(1)根据反应前后各原子的种类和数目不变,可知还缺少2个铁原子,4个氯原子,因为前面系数是2,所以化学式为:FeCl
2;一种单质和一种化合物反应生成另一种单质和另一种化合物的反应属于置换反应,该反应的生成物中没有单质,所以不属于置换反应;
(2)①反应前溶液中溶质为氯化铁质量为:1000g×16.25%=162.5g;
②设参加反应的铜的质量为X
Cu+2FeCl
3═CuCl
2+2FeCl
2
64 325
X 162.5g
根据:
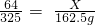
解得X=32,所以反应后所得溶液的质量为:32g+1000g=1032g.
故答案为:(1)FeCl
2;不属于;(2)①162.5g;②1032g.
分析:(1)根据质量守恒定律和置换反应的定义考虑本题;(2)①反应前溶液中溶质为氯化铁;②反应后所得溶液的质量就是增加了参加反应的铜的质量.
点评:解答本题的关键是利用质量守恒定律来求化学式,由于该反应没有产生沉淀、气体,所以反应后所得溶液的质量就是增加了参加反应的铜的质量.

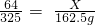 解得X=32,所以反应后所得溶液的质量为:32g+1000g=1032g.
解得X=32,所以反应后所得溶液的质量为:32g+1000g=1032g.

 省略).
省略).
