
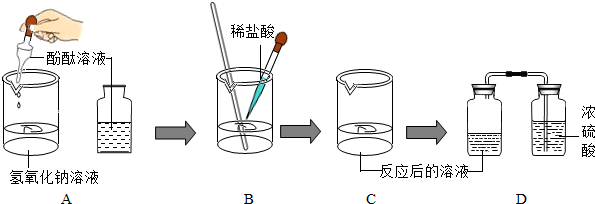
| 实验步骤 | 实验现象 | 实验结论 | |
| 步骤① | 取适量NaOH溶液放入烧杯中,滴入几滴酚酞试液. | ---------------------- | |
| 步骤② | 用胶头滴管将稀盐酸慢慢逐滴滴入到步骤①所得的溶液中,__________. | 溶液颜色逐渐变浅直到无色. | 氢氧化钠与稀盐酸反应. |
| 步骤③ | 当滴加稀盐酸至发生上述现象出现,立即停止. | -------------------- | ---------------------- |
| 步骤④ | 将③所得溶液移入广口瓶,并与盛有浓硫酸的广口瓶用导管连接导通,放置一段时间. | ______________. | ______________. |
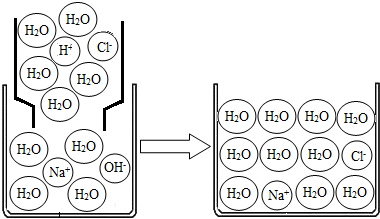
| 实验步骤 | 实验现象 | 实验结论 | |
| 步骤① | 溶液变红. | ---------------------- | |
| 步骤② | 边加边搅拌. | ||
| 步骤③ | --------------------- | ---------------------- | |
| 步骤④ | 有无色晶体析出. | 浓硫酸有吸水性. | |
| 58.5 |
| 58.5+18×10 |


科目:初中化学 来源: 题型:阅读理解
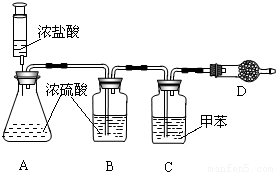
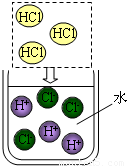
 26、盐酸是氯化氢(HCl)气体溶于水形成的溶液,HCl是极易溶于水的无色气体.如图为HCl气体溶于水的微观示意图.HCl气体也可溶于甲苯(一种有机溶剂),得氯化氢的甲苯溶液.
26、盐酸是氯化氢(HCl)气体溶于水形成的溶液,HCl是极易溶于水的无色气体.如图为HCl气体溶于水的微观示意图.HCl气体也可溶于甲苯(一种有机溶剂),得氯化氢的甲苯溶液.

| 实验内容 | 现象 | 解释 |
| 与氧化铜 作用 |
盐酸:① | 化学方程式:② |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢在甲苯中没有解离出氢离子 | |
| 与碳酸钙粉末作用 | 盐酸:粉末消失,产生气泡 | 化学方程式:③ |
| 氯化氢的甲苯溶液:④ | 氯化氢在甲苯中没有解离出氢离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 探究小组同学发现家中烧开水的铝壶和盛放开水的暖瓶,长时间使用会有白色固体附着,很难洗掉.
探究小组同学发现家中烧开水的铝壶和盛放开水的暖瓶,长时间使用会有白色固体附着,很难洗掉.| 实验步骤 | 实验现象与结论 |
| 在上述实验的试管中,加入 稀盐酸 稀盐酸 后,再将产生的气体通入澄清石灰水中 |
若有气泡产生且澄清石灰水变浑浊,则难溶物是 CaCO3 CaCO3 (或猜想1成立) |
| ||
| 该同学的观点 | 请说出你的观点并阐述理由 |
| ①该实验装置中C装置可以不要 | 不同意此观点,因为氧化钠溶液能吸收二氧化碳 不同意此观点,因为氧化钠溶液能吸收二氧化碳 |
| ②“结论2”不正确 | 同意此观点,根据质量守恒定律,反应前后原子的种类和数目不变,反应前有氢原子,反应后又无氢气生成,所以应有水生成. 同意此观点,根据质量守恒定律,反应前后原子的种类和数目不变,反应前有氢原子,反应后又无氢气生成,所以应有水生成. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| 1 |
| 5 |
| 1 |
| 5 |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2012届江苏省南通市海安县紫石中学九年级适应性考试化学试卷(带解析) 题型:探究题
(13分)化学是一门以实验为基础的学科,通过一年的学习,相信你的实验能力一定有了很大提高,请你一同参与回答以下问题。
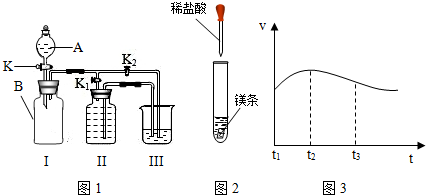
(一)某实验小组设计了下图所示的实验装置。
⑴ 写出仪器A的名称
⑵ 甲同学认为打开K1、关闭K2时,利用I、Ⅱ装置,可以制取并收集氧气,该化学反应方程式为 : 。
⑶乙同学认为利用Ⅰ、Ⅲ装置可以测定空气中氧气的含量。关闭K、K1、K2,用凸透镜引燃B中的白磷,待冷却后打开K2,整个实验过程中能观察到的现象是:① ;② 。
⑷ 丙同学认为可以利用Ⅰ、Ⅲ装置验证二氧化碳能与氢氧化钠溶液发生反应。他在广口瓶B中预先收集满二氧化碳气体,在仪器A中盛放氢氧化钠浓溶液,烧杯中盛放稀盐酸, K1关闭、K2打开,然后打开K将氢氧化钠浓溶液滴入广口瓶中,关闭K,依据 现象,可以证明二氧化碳能与氢氧化钠溶液发生化学反应。
(二)甲、乙两同学对有关镁与盐酸的反应进行了系列研究(如图)
探究一:镁与盐酸反应过程中的能量变化以及反应速率的变化:`
⑴实验时需将镁条进行打磨,其目的是 。
⑵反应中试管外壁发烫,说明镁与稀盐酸反应是放热反应,化学方程式为 。
⑶实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,你认为在t1~t2时间内反应速率逐渐加快的主要原因是: 。
探究二:.反应后所得溶液的酸碱性探究
【发现问题】
⑴反应后甲同学用pH试纸测定试管中溶液的酸碱性,发现pH小于7,说明甲同学所得溶液呈 性,(选填“酸”“碱”或“中”)。
⑵反应后乙同学的试管中镁条有剩余,向试液中滴入两滴酚酞溶液,溶液变红。
【查阅资料】氢氧化镁微溶于热水,且溶解度随温度升高而增大。
【提出猜想】
甲同学:猜想Ⅰ:稀盐酸过量,使溶液pH小于7;
猜想Ⅱ:氯化镁溶液pH小于7。
乙同学:猜想Ⅰ:氯化镁溶液呈碱性使酚酞变成红色;
猜想Ⅱ:镁与热水反应后生成碱使酚酞变红色。
【实验与思考】
⑴为验证猜想,甲、乙两同学均需测定____溶液的酸碱性,实验表明该溶液显弱酸性。
⑵乙同学为验证猜想Ⅱ,在滴有两滴酚酞的热水中放入一段打磨过的镁条,观察到溶液很快变为红色,同时还观察到镁条表面有气泡产生,收集并点燃该气体,发现气体能燃烧,请根据以上现象写出镁与热水反应的化学方程式 ;
⑶乙同学在进行上述猜想Ⅱ的探究时,发现实验一段时间后,酚酞的红色总是会逐渐消失,于是他猜想可能是镁与热水反应后生成的碱逐渐被空气中的二氧化碳反应掉了,但甲同学猜想可能是水温逐渐降低,导致 ,请你设计一个简单的实验方案验证甲或乙的猜想是否成立 (写出相应的操作、现象和结论): 。
【结论】
镁与稀盐酸反应,若镁反应完全后所得溶液显酸性,若镁过量时所得溶液显碱性。
查看答案和解析>>
科目:初中化学 来源:2010年江苏省无锡市蠡园中学中考化学二模试卷(解析版) 题型:填空题
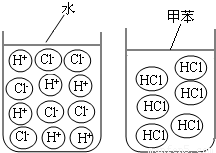
| 实验内容 | 现象 | 解释 |
| 与氧化铜 作用 | 盐酸:① | 化学方程式:② |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢在甲苯中没有解离出氢离子 | |
| 与碳酸钙粉末作用 | 盐酸:粉末消失,产生气泡 | 化学方程式:③ |
| 氯化氢的甲苯溶液:④ | 氯化氢在甲苯中没有解离出氢离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com