
| A. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | B. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$CO2↑+2Cu | ||
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | D. | Al(OH)3+3HCl═AlCl3+3H2O |
分析 置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,据此进行分析判断.
解答 解:A、S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,该反应符合“多变一”的特征,属于化合反应,故选项错误.
B、C++2CuO$\frac{\underline{\;高温\;}}{\;}$CO2↑+2Cu,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项正确.
C、2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该反应符合“一变多”的特征,属于分解反应,故选项错误.
D、Al(OH)3+3HCl═AlCl3+3H2O,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项错误.
故选:B
点评 本题难度不大,掌握置换反应的特征(“单化变单化”)是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 溶质的质量分数与原溶液相同 | B. | 溶剂的质量与原溶液相等 | ||
| C. | 溶质的质量比原溶液增加了 | D. | 析出固体后的溶液是不饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
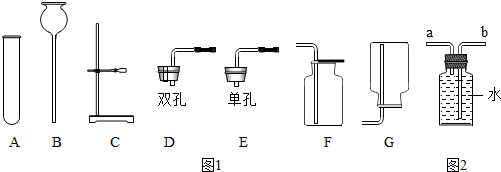
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 解释与结论 |
| ①取少量澄清废液于试管中,逐滴加入足量氢氧化钠溶液 | 刚开始没有明显现象,过一段时间后产生红褐色沉淀 | 生成的红褐色沉淀是氢氧化铁 |
| ②过滤,向滤液中滴加氯化钡溶液 | 有白色沉淀产生 | 该厂除铁锈用了稀硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用活性炭可除去水中色素和臭味 | B. | 水是无色无味、澄清透明的液体 | ||
| C. | 向水中加入硫酸钠会增强导电性 | D. | 地球上的淡水资源是无限的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | B | C | D | |
| 区分的物质 | 蒸馏水和 医用酒精 | 区分黄铜和黄金 | 氢氧化钠和氢氧化钙 | 区分空气和人体呼出的气体 |
| 方案一 | 测pH | 观察颜色 | 在空气中放置一段时间后观察 | 取样,分别插入带火星木条 |
| 方案二 | 取样涂抹在皮肤上 | 取样,分别加入稀盐酸 | 加水溶解观察 | 取样,分别加入澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com