
【题目】某化学小组同学利用盐酸和氧化铜进行实验的过程中,出现了意想不到的现象:发现溶液变为了绿色。为探究溶液变绿的原因,进行系列实验。
(查阅资料)①氧化铜(CuO)为黑色固体②铜离子(Cu2+)在水溶液中呈蓝色
(进行实验)
实验1:取2mL不同浓度的盐酸分别加入到盛有0.2g氧化铜的试管中,进行实验。
序号 | 浓盐酸与水的体积比 | 现象 |
1-1 | 1:1 | 30秒后溶液变为绿色,无黑色固体剩余 |
1-2 | 1:2 | 1分钟后溶液变为蓝绿色,无黑色固体剩余 |
1-3 | 1:3 | 2分钟后溶液变为蓝色,无黑色固体剩余 |
1-4 | 1:4 | 4分钟后溶液变为浅蓝色,有黑色固体剩余且不再减少 |
实验2:取2mL稀盐酸(浓盐酸与水的体积比为1:3)加入到盛有0.2g氧化铜的试管中,实验装置如下。
序号 | 2-1 | 2-2 |
操作 |
|
|
现象 | 2分钟后溶液变为蓝色,无黑色固体剩余 | 10秒后溶液变为浅绿色,无黑色固体剩余 |
(解释与结论)
(1)补全氧化铜与盐酸反应的化学方程式:![]() _____
_____
(2)实验1中配制不同浓度的盐酸时,需要使用的仪器包括_____(填序号,下同)。
A 量筒
B 烧杯
C 玻璃棒
D 酒精灯
(3)实验1的目的是_____。
(4)结合实验1和实验2,得出的结论是_____。
(反思与评价)
(5)实验1-4中,“有黑色固体剩余”的原因是_____。
(6)实验1中若进行浓盐酸与水的体积比为1:5的实验,充分反应后可能出现的现象为_____。
A 溶液变为绿色,无黑色固体剩余
B 溶液变为更浅的蓝色,有黑色固体剩余
C 溶液变为更浅的蓝色,无黑色固体剩余
【答案】H2O ABC 探究盐酸的浓度与反应速率的关系 反应物的浓度越大,温度越高,反应速率越快 盐酸的量不足,没有将氧化铜完全反应掉 B
【解析】
解释与结论:(1)根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含1个铜原子、1个氧原子、2个氢原子,2个氯原子,生成物中含有1个铜原子、2个氯原子,故还应含有1个氧元素,2个氢原子,故还有水生成,将化学方程式补全为:![]() ;
;
(2)用浓溶液配制稀溶液需要用到的仪器有:量筒(量取所需的水和浓盐酸)、玻璃棒(搅拌)、烧杯(溶解仪器)、胶头滴管。
故选ABC;
(3)由实验1可知,该实验将浓盐酸配制成不同浓度的稀盐酸,然后取2mL不同浓度的盐酸分别加入到盛有0.2g氧化铜的试管中,然后记录溶液变色的时间,变量是盐酸的浓度,故该实验是探究盐酸的浓度与反应速率的关系;
(4)由实验1可知,盐酸浓度越大,溶液变色的时间越短,说明盐酸浓度越大,反应速率越快;
实验2:取2mL稀盐酸(浓盐酸与水的体积比为1:3)加入到盛有0.2g氧化铜的试管中,常温下,2分钟后溶液变为蓝色,无黑色固体剩余,加热时,10秒后溶液变为浅绿色,无黑色固体剩余,说明温度越高,反应速率越快。
故结合实验1和实验2,得出的结论是:反应物的浓度越大,温度越高,反应速率越快;
反思与评价:(5)实验1-4中,“有黑色固体剩余”,可能是盐酸的浓度过小,盐酸的量不足,没有将氧化铜完全反应掉,故填:盐酸的量不足,没有将氧化铜完全反应掉;
(6)由实验1可知,盐酸的浓度越小,反应生成溶液的颜色越浅,盐酸浓度越小,盐酸的量越不足,浓盐酸与水的体积比:1:4时,4分钟后溶液变为浅蓝色,有黑色固体剩余且不再减少,故浓盐酸与水的体积比为1:5时,溶液颜色会变为更浅的蓝色,黑色固体有剩余。
故选B。


科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的溶解度曲线,如图所示,回答下列问题:

(1)P点的含义_____;
(2)当乙中混有少量甲时,可采用_____(填“降温结晶”或“蒸发结晶”)的方法提纯乙。
(3)t2℃时,将甲、乙、丙三种物质的饱和溶液同时降温到t1℃,所得溶液中溶质质量分数由大到小的顺序为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 化学与杜会生活
(1)从铁、生石灰、烧碱、小苏打、硫酸铜中选择符合题意的物质(用化学式填空)。常用来配制波尔多液的盐是_____,焙制糕点所用的发酵粉的主要成份是_____。
(2)生活中常用二氧化碳灭火而不用氮气灭火的原因是_____。
化学与传统文化
(3)北宋《浸铜要略序》载“山麓有胆泉(硫酸铜溶液),土人汲以浸铁,数日辄类朽木,刮取其屑,锻炼成铜”,请用化学方程式表示其原理_____。
(4)《汉代古火井碑序》记载:“诸葛丞相躬莅视察,改进技法,刳斑竹以导气(气指天然气),引井火以煮盐”,请用化学方程式表示其原理_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请帮助小红利用下列实验装置制备并研究CO2的性质
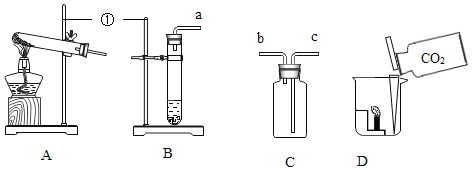
(1)仪器①的名称是____,装入药品之前应先进行的操作是____。
(2)实验室里制取一瓶CO2气体,应选择的气体发生装置是____(填“A”或“B”)。按气体从左到右流动,导管口的连接顺序是a→____→____(填接口小写字母)。检验本实验中CO2已经收集满的操作是____。
(3)将收集到的CO2气体按图D进行实验,可观察到蜡烛熄灭。通过该实验可知CO2具有的性质是____(填字母序号)。
a.密度比空气大 b.既不能燃烧也不支持燃烧
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下图装置进行实验。升温至60℃的过程中,仅①燃烧;继续升温至260℃的过程中,仅③燃烧。下列分析不正确的是( )
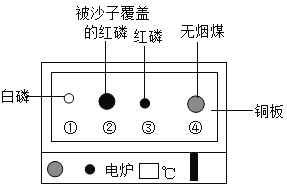
A. ①燃烧,说明白磷是可燃物
B. 对比①③,可说明红磷的着火点比白磷的高
C. 对比②③,可验证燃烧需可燃物与氧气接触
D. ④未燃烧,说明无烟煤不是可燃物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合图示实验装置,回答下列问题。
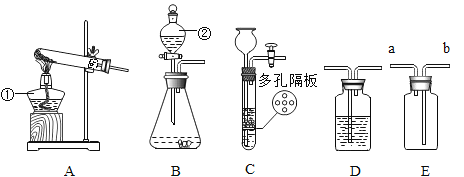
(1)请写出图中标有字母的仪器名称:②________________________________。
(2)实验室用高锰酸钾制取氧气,反应的化学方程式是__________________________。
(3)若用B装置制H2。要获得干燥的H2,应先将气体通过盛有_____________的D装置, 再用E装置收集,气体应从_______________端通入(选填“a”或“b”)。
(4)实验室用大理石和稀盐酸来制二氧化碳,C相对于B装置的优点有__________________________。
(5)实验室常用氯化铵固体与碱石灰固体共热来制取一种易溶于水密度比空气小的氨气(NH3),应选择的制备和发生装置是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种物质的溶解度曲线,下列说法正确的是
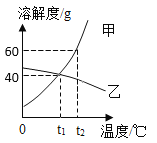
A.将乙物质的不饱和溶液转化为饱和溶液,可采用降低温度的方法
B.t1°C时,50 g甲物质加入100 g水中,充分搅拌,得到150 g溶液
C.将t1°C时的乙物质的饱和溶液升温至t2°C ,有结晶现象
D.t2°C时,甲物质的饱和溶液中溶质质量分数为60%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与我们的生活密切相关,请用学过的化学知识回答:
(1)请用化学式填写下列生活中涉及的物质:新能源燃料氢能的主要成分____________;家里厨房食醋的主要成分____________;用于建筑材料的大理石____________;用于制温度计的水银____________。
(2)大雾天导致呼吸道病人增多,因为雾霾可使空气中增加大量的____________。
A二氧化氮 B二氧化硫 C一氧化碳 D可吸入颗粒物
(3)为防止雾霾影响,PM2.5口罩中使用了活性炭,这是利用了活性炭的____________ 作用。
(4)为了减少对大气的污染,全国很多省市都提倡使用压缩天然气汽车,简称CNG汽车,请写出甲烷燃烧的化学方程式:____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】粗盐中除了含有泥沙等难溶性物质外,还含有可溶性杂质Na2SO4、MgCl2和CaCl2为了除去其中的可溶性杂质,某化学兴趣小组设计了如图实验过程。
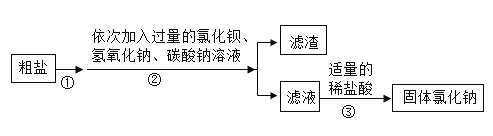
(1)①②③操作中都要用到的一种玻璃仪器是_______________。
(2)Na2CO3需要在BaCl2之后加入,为什么?_________
(3)最终得到的氯化钠固体与粗盐中含有的氯化钠相比,质量增加,请写出导致这一变化的化学方程式。(写出一个)_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com