
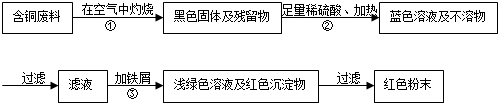
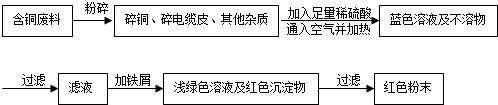
分析 根据铜能与氧气反应生成氧化铜,生成的氧化铜可以与酸反应生成盐和水,在金属活动性顺序中,氢前的金属能与酸反应生成盐和氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,要回收铜可以加入活动性比铜强的金属等知识进行分析.
解答 解:(1)反应③是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═FeSO4+Cu;
(2)从环保角度对两套方案的不同部分进行比较,甲方案第一步灼烧会产生污染空气的气体,粉尘,烟雾,由此可知乙的方案更合理;
(3)加入略过量的铁屑,是将硫酸铜全部置换出来;如果铁过量,会混在红色粉末中,可以加入适量的酸除去剩余的铁屑;
(4)“绿矾”溶解度随温度升高而增大,所以结晶的方法有:蒸发结晶.
故答案为:(1)①Fe+CuSO4=FeSO4+Cu;
(2)乙,甲方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾;
(3)确保CuSO4 反应完;将所得铜粉酸洗后再洗涤、干燥;
(4)蒸发结晶.
点评 本题探讨了“从含铜废料中回收铜”的有关问题,设计了不同的方案,并进行评价,考察了考生的思考、探讨、评价等诸多能力.


 53天天练系列答案
53天天练系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 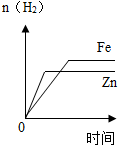 分别向质量相等的铁片和锌片中滴加过量的稀硫酸 | |
| B. | 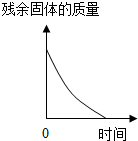 加热一定质量的高锰酸钾 | |
| C. |  某温度下,向一定质量的饱和硝酸钾中不断加入硝酸钾晶体 | |
| D. | 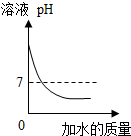 向一定质量的NaOH溶液中滴加水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | C24H38O4中碳、氢、氧元素质量比为12:19:2 | |
| B. | 邻苯二甲酸二辛酯中碳元素的质量分数最大 | |
| C. | C24H38O4由24个碳原子、38个氢原子、4个氧原子构成 | |
| D. | 邻苯二甲酸二辛酯属于氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
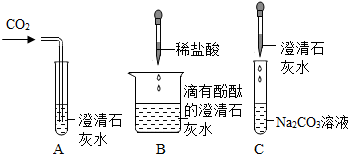 如图所示是Ca(OH)2的部分性质实验,回答有关问题.
如图所示是Ca(OH)2的部分性质实验,回答有关问题.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | K+、MnO4-、Cu2+、SO42- | B. | Na+、CO32-、NO3-、Cl | ||
| C. | K+、Cu2+、SO42-、HCO3- | D. | K+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
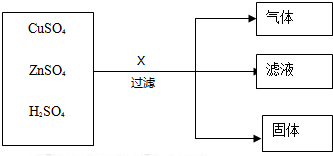
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com