
分析 (1)根据配制溶质质量分数一定的溶液的基本步骤,进行分析解答.
(2)根据溶质的质量=溶液的质量×溶质的质量分数来分析;
(3)根据溶质的质量分数的计算方法来分析;
(4)根据溶质质量分数公式可以求得溶液的质量,从而求得水的质量,再根据密度公式计算水的体积,砝码缺少一角则称量的食盐的质量减小,可以据此解答该题.
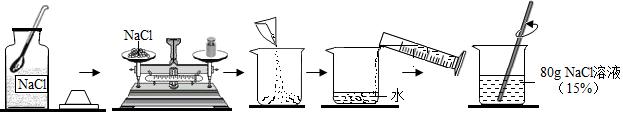
解答 解:(1)配制一定溶质质量分数的氯化钠溶液,首先计算配制溶液所需NaCl和水的质量,再称量所需的NaCl和量取水,进行溶解,最后装瓶存放;
(2)氯化钠的质量为:80g×15%=12g;需要水的质量为:80g-12g=68g,需要水的体积为68g÷1g/mL=68mL;在溶解过程中玻璃棒搅拌的目的是加速溶解;
(3)溶质的质量分数为:$\frac{10g×15%}{10g+40g}×100%$=3%;
(4)砝码缺少一角则称量的食盐的质量减小,溶质减少,则溶液变稀,溶质质量分数变小.
故答案为:(1)计算;溶解;(2)12;68;加速溶解;(3)3%;(4)小于.
点评 本题考查了溶液的配制,完成此题,可以依据已有的知识结合溶质质量分数公式进行.


科目:初中化学 来源: 题型:选择题
| A. | 分别加入适量澄清石灰水 | B. | 将普通木条分别伸入瓶中 | ||
| C. | 将燃着的木条分别伸入瓶中 | D. | 分别加入蒸馏水 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 向溶液中加入20g蔗糖 | |
| B. | 将溶液加热蒸发掉50g水 | |
| C. | 向溶液中加入100g溶质质量分数是30%的蔗糖溶液 | |
| D. | 向溶液中加入50g溶质质量分数是10%的蔗糖溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 客观事实 | 微观解释 |
| A | 品红在热水中扩散比在冷水中快 | 水分子间存在间隙 |
| B | H2O 在通电条件下产生 H2 | H2O 分子中存在 H2 |
| C | NaOH 固体溶于水放热 | Na+、OH-与水分子形成水合离子过程中放出的热量大于Na+、OH-向水分子中扩散过程中吸收的热量 |
| D | 搅拌能加快蔗糖在水中的溶解 | 搅拌使蔗糖分子在水中溶解更多 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 广西矿产资源丰富,铟的生产规模居世界同类企业首位,图1是元素周期表中铟元素的信息,图2是铟原子的结构示意图,回答下列问题:
广西矿产资源丰富,铟的生产规模居世界同类企业首位,图1是元素周期表中铟元素的信息,图2是铟原子的结构示意图,回答下列问题: .它与铟元素的族 数相同.
.它与铟元素的族 数相同.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成氮化镁(Mg3N2),设计了如下方案进行验证.
某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成氮化镁(Mg3N2),设计了如下方案进行验证.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 结论 | 总结 | |||
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是反应慢. | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气. | |
| 实验三 | 向盛有5mL5%过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条 | 有大量气泡产生,带火星的木条迅速复燃. | 二氧化锰能加快过氧化氢的分解,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com