




 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源:不详 题型:实验题
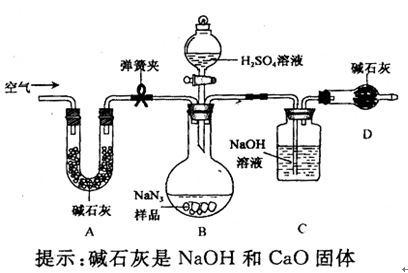
 (NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热。
(NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热。
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 试管 | A | B | C | D | E | F |
| CuSO4溶液/毫升 | 0 | 0.5 | 1 | 1.5 | 2 | 4 |
| 水/毫升 | 4 | 3.5 | 3 | V1 | V2 | 0 |
| 收集H2所用的时间/秒 | 348 | 246 | 190 | 165 | 230 | 360 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.提出假设 | B.交流评价 | C.设计实验 | D.作出结论 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com