
【题目】以下是在实验室里制取气体时常用的部分仪器。

(1)标号为E的仪器名称是_____;
(2)在实验室里,用2H2O2![]() 2H2O+O2↑来制取并用排水法收集氧气。
2H2O+O2↑来制取并用排水法收集氧气。
①应选用图中A、C、D、H、M、N、O和_____来组装装置;
②若制取3.2g氧气,理论上至少需要取10%过氧化氢溶液_____g;
③当集气瓶口有气泡向外逸出时,取出导管,接下来对集气瓶的处理操作是_____。
【答案】酒精灯 F、L 68 在水面以下盖上玻璃片,正放在桌面上
【解析】
制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热。氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集。
(1)酒精灯是常用的加热仪器。
(2)在实验室里,用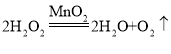 来制取并用排水法收集氧气;①应选用图中A、C、D、H、M、N、O和F、L来组装装置;
来制取并用排水法收集氧气;①应选用图中A、C、D、H、M、N、O和F、L来组装装置;
②设理论上至少需要取10%过氧化氢溶液的质量为x;
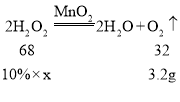
![]()
x=68g
故理论上至少需要取10%过氧化氢溶液68g。
③当集气瓶口有气泡向外逸出时,取出导管,接下来对集气瓶的处理操作是:在水面以下盖上玻璃片,正放在桌面上。


 天天向上口算本系列答案
天天向上口算本系列答案科目:初中化学 来源: 题型:
【题目】为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:
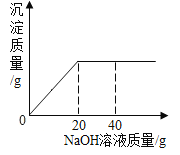
请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数为_________(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】经过多方努力,安徽省各地市的空气质量有明显改善。造成雾霾的重要原因之一是汽车尾气的排放,汽车加装尾气处理装置可以减少有害气体的排放。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作区用的微观示意图如图所示。下列说法错误的是( )
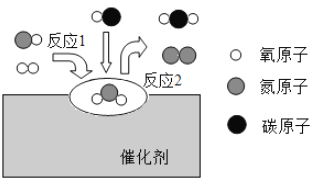
A. 反应中没有发生变化的是碳原子、氮原子和氧原子
B. 可解决汽车尾气带来的空气污染问题
C. 该微观示意图中涉及四种氧化物
D. 反应1的化学方程式为NO+O2=NO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验室中利用下列仪器进行制取气体的实验,请回答下列问题:
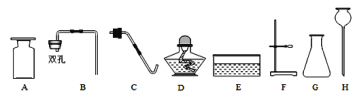
(1)仪器G的名称是___________;
(2)利用图中仪器可以制取并收集二氧化碳,你选择的仪器是________________(填字母)。
(3)小雅想要检验收集的气体是二氧化碳,她应该将气体通入_________________中。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】回答下列与含碳物质有关的问题:
(1)在金刚石和石墨中,能用于制作干电池电极的是_____;
(2)利用活性炭除去除去冰箱中的异味,利用了活性炭的_____性;
(3)工业上用煅烧石灰石的方法制取CO2,该反应的化学方程式为_____;
(4)碳和水蒸气高温下反应生成氢气和一氧化碳,其中_____发生氧化反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
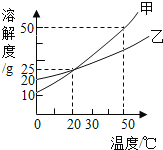
A. 20℃时,100g甲饱和溶液中含甲物质的质量是25g
B. 20℃时,等质量甲、乙两种溶液中含溶质的质量相等
C. 甲物质的溶解度大于乙物质的溶解度解
D. 50℃时,将甲、乙两种物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数一定相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D是初中化学常见的物质,他们的关系如图:“一”表示相互之间可以反应,“→”表示可以转化生成。其中A是年产量最多的金属,C是一种常见的碱,B和C反应生成的一种物质是我们日常生活的调味品,D是一种气体,D在大气中含量的增加会导致温室效应。

(1)写出D的化学式_____;写出物质C的一种用途_____。
(2)写出A和B反应的化学方程式_____;该反应属于_____类型(从①化合反应②分解反应③置换反应④复分解反应中选择)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属锶用于冶金、电子、化学和蓄电池等工业,是制取各类锶合金的优质原料.锶元素的原子结构示意图和元素周期表中显示的信息如图所示.下列说法错误的是( )

A. 锶原子的核外共有5个电子层,最外层有2个电子
B. 锶的原子序数为38,属于非金属元素
C. 锶的相对原子质量为87.62,原子核内质子数为38
D. 锶原子在化学反应中易失去电子,形成Sr2+
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某课外活动小组同学用图中装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体)。实验过程如下:
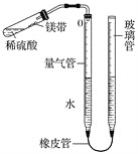
①取一段镁带样品,准确称得其质量为0.030 g;
②往量气管内装水至低于刻度“0”的位置,如图所示,(未装药品)装配好仪器;
③_________________________;
④在试管中加入足量的稀硫酸,稍倾斜试管,将用水湿润的镁带小心贴在试管壁上,塞紧橡皮塞;
⑤调整量气管液面,使两边的液面保持同一水平,记录量气管中液面位置;
⑥把试管底部略为抬高,使镁带与稀硫酸接触完全反应;
⑦待冷却至室温后,再次记录量气管中液面位置;
⑧算出量气管中增加的气体体积为23.96 mL;
已知:同温同压下,不同气体混合后体积等于混合前各气体体积之和。
请回答下列问题:
(1)写出镁与稀硫酸反应的化学方程式:____________________。
(2)能否用托盘天平称量0.030 g镁带样品________(填“能”或“不能”)。
(3)操作③是_________________________。
(4)实验过程⑦中再次记录量气管的液面位置时,试管中留有氢气,是否会影响实验最终结果________(填“是”或“否”),理由是_______________________。
(5)若实际测得氢气的体积与理论值相比偏大,则可能的原因是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com