
°æƒø°øœ¬±Ì «¬»ªØƒ∆∫ÕúÀ·ƒ∆‘⁄≤ªÕ¨Œ¬∂» ±µƒ»‹Ω‚∂»£¨∏˘æ›¥À±Ìªÿ¥£∫
Œ¬∂»/°Ê | 10 | 20 | 30 | 40 | |
»‹Ω‚∂»/g | ¬»ªØƒ∆ | 35.8 | 36.0 | 36.3 | 36.6 |
úÀ·ƒ∆ | 12.2 | 21.8 | 39.7 | 53.2 | |
£®1£©40°Ê ±£¨¬»ªØƒ∆µƒ»‹Ω‚∂»Œ™________g°£
£®2£©ÃºÀ·ƒ∆»‹“∫÷–ªÏ”–…Ÿ¡øµƒ¬»ªØƒ∆£¨ø…Õ®π˝________Ω·æß∑Ω∑®Ã·¥ø°£
£®3£©‘⁄20°Ê ±£¨‘⁄100gÀÆ÷–º”»Î25 gúÀ·ƒ∆£¨≥‰∑÷Ω¡∞Ë∫Ûµ√µΩµƒ «_____£®ÃÓ°∞±•∫Õ°±ªÚ°∞≤ª±•∫Õ°±£©»‹“∫£¨Ω´…œ ˆ»‹“∫…˝Œ¬µΩ30°Ê£¨À˘µ√»‹“∫µƒ»‹÷ ÷ ¡ø∑÷ ˝Œ™________°£
°æ¥∞∏°ø 36.6 ΩµŒ¬ ±•∫Õ 20%
°æΩ‚Œˆ°ø∏˘æ›À˘—ß÷™ ∂∫ÕÂ÷––≈œ¢÷™£¨£®1£©40°Ê ±£¨¬»ªØƒ∆µƒ»‹Ω‚∂»Œ™36.6g. £®2£©ÃºÀ·ƒ∆»‹“∫÷–ªÏ”–…Ÿ¡øµƒ¬»ªØƒ∆£¨ø…Õ®π˝ΩµŒ¬Ω·æß∑Ω∑®Ã·¥ø°££®3£©‘⁄20°Ê ±£¨ÃºÀ·ƒ∆»‹Ω‚∂» «21.8∏ˆ£¨‘⁄100gÀÆ÷–º”»Î25 gúÀ·ƒ∆£¨≥‰∑÷Ω¡∞Ë∫Ûµ√µΩµƒ «±•∫Õ»‹“∫£¨Ω´…œ ˆ»‹“∫…˝Œ¬µΩ30°Ê£¨ÃºÀ·ƒ∆»‹Ω‚∂» «39.7∏ˆ£¨À˘µ√»‹“∫µƒ»‹÷ ÷ ¡ø∑÷ ˝Œ™°√![]() °¡100%£Ω20%°£
°¡100%£Ω20%°£
µ„涰√±æÂ÷˜“™øº≤È”–πÿ»‹Ω‚∂»µƒ÷™ ∂°£



| ƒÍº∂ | ∏fl÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏fl“ª | ∏fl“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏fl∂˛ | ∏fl∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏fl»˝ | ∏fl»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫≥ı÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬¡–”–πÿΩ ÙµƒÀµ∑®÷–’˝»∑µƒ «
A£Æ≥£Œ¬œ¬Ω Ù∂º «πÃÃÂ
B£ÆΩ Ù∂º «“‘ªØ∫œŒÔ–Œ Ω¥Ê‘⁄”⁄◊‘»ªΩÁ÷–
C£Æ…˙Ã˙∫Õ∏÷∂º «Ã˙µƒ∫œΩ£¨∆‰÷–…˙Ã˙µƒ∫¨Ãº¡ø¥Û”⁄∏÷
D£Æ¬¡‘⁄≥£Œ¬œ¬æÕƒ‹”Ηı∆¯∑¥”¶£¨À˘“‘¬¡÷∆∆∑∫‹»›“◊–‚ ¥
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫≥ı÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø≥˝»•œ¬¡–ŒÔ÷ ÷–∫¨”–µƒ…Ÿ¡ø‘”÷ £¨À˘—°”√µƒ ‘º¡∫Õ≤Ÿ◊˜∑Ω∑®æ˘’˝»∑µƒ «
—°œÓ | ŒÔ÷ £®¿®∫≈ƒ⁄Œ™‘”÷ £© | ‘º¡ | ≤Ÿ◊˜∑Ω∑® |
A | CaCO3£®CaO£© | Œfi | ∏flŒ¬ |
B | CO2£®CO£© | O2 | µ„»º |
C | CuO£®Õ≠∑€£© | ◊„¡ø—ı∆¯ | ◊∆…’ |
D | KCl£®KClO3£© | ∂˛—ıªØ√à | º”»» |
A. A B. B C. C D. D
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫≥ı÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø∞¢Àæ∆•¡÷µƒªØ—ß ΩŒ™C9H8O4£¨œ¬¡–πÿ”⁄∞¢Àæ∆•¡÷µƒÀµ∑®÷–£¨’˝»∑µƒ «
A. À¸ Ù”⁄—ıªØŒÔ
B. œ‡∂‘∑÷◊”÷ ¡øŒ™180
C. ∞¢Àæ∆•¡÷÷–«‚°¢—ı‘™Àÿµƒ÷ ¡ø±»Œ™2©U1
D. 1∏ˆ∞¢Àæ∆•¡÷∑÷◊”÷–∫¨4∏ˆH2∑÷◊”£¨2∏ˆO2∑÷◊”
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫≥ı÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øÃ˙º∞∆‰∫œΩ «»’≥£…˙ªÓ◊Ó≥£”√µƒΩ Ù≤ƒ¡œ£¨”√Õæ∑«≥£π„∑∫°£«Îªÿ¥œ¬¡–Œ £∫
(1)»ÁÕº «“ª∞¸ø檮…˙µƒÕº∆¨£¨¥¸ƒ⁄µƒÕ——ıº¡∂‘ ≥∆∑±£÷ ∆¡À∑«≥£÷ÿ“™µƒ◊˜”√°£»°…Ÿ¡øÕ——ıº¡”⁄ ‘π‹÷–£¨µŒº”◊„¡øœ°—ŒÀ·µƒœ÷œÛ «______________________________________£ªÕ——ıº¡µƒ◊˜”√‘≠¿Ì «∆‰÷–µƒÃ˙∑€”Ηı∆¯°¢ÀÆ∑¢…˙∑¥”¶…˙≥…«‚—ıªØÃ˙£¨∏√∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™__________£ªæ›¥À≈–∂œÕ——ıº¡∂‘ ≥∆∑æfl”–∑¿∏ر£œ ◊˜”√µƒ‘≠“Ú «________________£®ÃÓ–Ú∫≈£©°£
a.Õ——ıº¡æfl”–…±æ˙°¢œ˚∂浃◊˜”√
b.Õ——ıº¡Œ¸ ’ÀÆ∑÷£¨ π ≥∆∑±£≥÷∏…‘Ô
c.Õ——ıº¡Œ¸ ’—ı∆¯£¨∑¿÷π ≥∆∑∑¢…˙ª∫¬˝—ıªØ

(2)œ¥œ‡“∫÷–∫¨”–Ωœ∂‡µƒœıÀ·“¯£¨Õ®≥£ π”√Ã˙Ω´∆‰÷√ªª≥ˆ¿¥£¨œ‡”¶µƒªØ—ß∑¥”¶∑Ω≥Ã Ω «
___________________________________________________£ª
(3)𧓵…œ÷˜“™¿˚”√“ª—ıªØú∏flŒ¬ªπ‘≠≥‡Ã˙øÛ(÷˜“™≥…∑÷Œ™—ıªØÃ˙)¿¥¡∂Ã˙£¨∆‰ªØ—ß∑Ω≥Ã ΩŒ™__________________________________________£ª”√1000t∫¨—ıªØÃ˙80%µƒ≥‡Ã˙øÛø…“‘¡∂≥ˆ∫¨Ã˙96%µƒ…˙Ã˙______________t°£(Ω·π˚±£¡Ù1Œª–° ˝)
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫≥ı÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øŒ“»œ ∂¡À–Ì∂‡ªØ—ß÷Æ◊Ó£®«Î”√ªØ—ß”√”ÔÃÓø’£©£∫
£®1£©ø’∆¯÷–∫¨¡ø◊Ó∂‡µƒ∆¯Ãµ•÷ «_________£ª
£®2£©µÿø«÷–∫¨¡ø◊Ó∏flµƒΩ Ù‘™Àÿ «_________°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫≥ı÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø”–“ª∆ø±Í«©±ª∏Ø ¥µƒœ°¡ÚÀ·£¨–°Ω≠Œ™¡À≤‚∂®»‹“∫÷–»‹÷ µƒ÷ ¡ø∑÷ ˝£¨”√NaOHπÃÃÂ∫ÕÀÆ≈‰÷∆40g 10%µƒNaOH»‹“∫”⁄…’±≠÷–£¨»ª∫ÛÕ˘…’±≠÷–µŒº”œ°¡ÚÀ·£¨∑¥”¶π˝≥Ã÷–»‹“∫µƒpH”εŒ»Îœ°¡ÚÀ·µƒ÷ ¡øπÿœµœ¬ÕºÀ˘ æ£∫
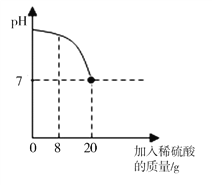
«Îº∆À„£∫£®“—÷™£∫2NaOH+ H2SO4= Na2SO4+2H2O£©
£®1£©≈‰÷∆40g 10%µƒNaOH»‹“∫£¨–Ë“™ÀƵƒ÷ ¡øŒ™ g£ª
£®2£©∏√œ°¡ÚÀ·÷–H2SO4÷ ¡ø∑÷ ˝£®–¥≥ˆº∆À„π˝≥ã©°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫≥ı÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øæ›”¢π˙°∂◊‘»ª°∑‘”÷æ±®µ¿£¨ø∆—ߺ“◊ÓΩ¸—–÷∆≥…¡À“‘Ô»‘≠◊”◊ˆ÷”∞⁄µƒ°∞π‚æß∏Ò÷”°±£¨≥…¡À ¿ΩÁ…œ◊Óæ´»∑µƒ÷”°£“—÷™“ª÷÷Ô»‘≠◊”µƒœ‡∂‘‘≠◊”÷ ¡øŒ™88£¨∆‰÷ ◊” ˝ «38£¨‘Ú’‚÷÷Ô»‘≠◊”µƒ∫ÀÕ‚µÁ◊” ˝Œ™( )°£
A°¢38 B°¢50 C°¢88 D°¢126
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫≥ı÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬±Ì «KCl∫ÕKNO3‘⁄≤ªÕ¨Œ¬∂»œ¬µƒ»‹Ω‚∂»°£œ¬¡–Àµ∑®≤ª’˝»∑µƒ «
Œ¬∂»/ °Ê | 20 | 30 | 40 | 50 | |
»‹Ω‚∂»/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
A. 35°Ê ±£¨KClµƒ»‹Ω‚∂»–°”⁄KNO3µƒ»‹Ω‚∂»
B. 40°Ê ±£¨ KCl±•∫Õ»‹“∫µƒ»‹÷ ÷ ¡ø∑÷ ˝Œ™40%
C. ¡Ω÷÷ŒÔ÷ »‹Ω‚∂»œ‡µ»µƒŒ¬∂»‘⁄20~30°Ê÷ƺ‰
D. 50°Ê ±£¨185.5g KNO3±•∫Õ»‹“∫ΩµŒ¬µΩ20°Ê£¨Œˆ≥ˆ53.9gKNO3 æßÃÂ
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒfi÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com