
【题目】如表为氯化钠和硝酸钾的溶解度:
10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ | |
NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
(1)60℃时,KNO3的溶解度为_____;表中“37.8”的意义是 _____。
(2)20℃时KNO3 的溶解度_____(选填“大于”“小 于”)NaCl的溶解度。随着温度升高,NaCl的溶解度 _____(选填“变大”“变小”或“不变”)。
(3)20℃时,完全溶解18 g NaCl 恰好得到饱和溶液,所需水的质量是 _____g,该溶液质量分数为 _____。
(4)20℃时,向 10 g KNO3 固体不断加水,有关图像正确的是_____(选填编号)。
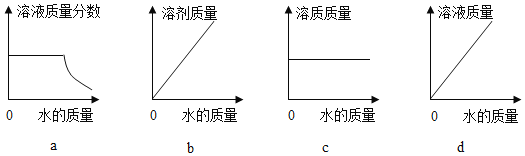
【答案】110g 70℃时,在100g水中达到饱和时,可溶解37.8g氯化钠 小于 变大 50 26.5% ab
【解析】
(1)60℃时,KNO3 的溶解度为110g;表中“37.8”的意义是:在70℃时,氯化钠的溶解度为37.8g,即70℃时,在100g水中达到饱和时,可溶解37.8g氯化钠;
(2)由表格中数据可知,20℃时 KNO3 的溶解度为31.6g,小于NaCl 的溶解度36.0g。随着温度升高,NaCl 的溶解度变大;
(3)20℃时,NaCl 的溶解度为36.0g,完全溶解 18g NaCl 恰好得到饱和溶液,所需水的质量是 50 g,该溶液质量分数为 ![]() ;
;
(4)20℃时,向10g KNO3固体不断加水,开始加水时,硝酸钾未完全溶解,所以开始溶液是饱和的,硝酸钾完全溶解后,随着水的加入,溶液的溶质质量分数不断减小;而溶液中溶剂的质量随着水的增大而不断增大;溶液中溶质的质量随着硝酸钾的溶解由小到大,完全溶解后溶质的质量不再改变;当硝酸钾未完全溶解时,随着水的加入溶液的质量增大,当硝酸钾完全溶解后,溶液的质量还是随着水的加入而增大,但是增大的幅度变小;故选ab。


科目:初中化学 来源: 题型:
【题目】对知识的归纳与整理是学习化学的一种重要方法.现有下列三个化学反应,请分别写出它们的文字表达式:
(1)碳燃烧________________;
(2)磷燃烧____________;
(3)石蜡燃烧_______________。
通过比较我们发现:它们有许多相似之处,其一________,其二__________。我能另写一个符合这两点的化学反应的文字表达式:___________;它们之间也存在相异之处,其中有一个反应与众不同,这个反应的不同之处是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室现有石灰石、稀盐酸、火柴、药匙、升降台、木条、棉花、镊子及以下仪器:
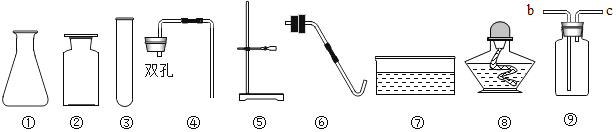
(1)若要制取CO2,应选择的仪器有①锥形瓶和_____(从①—⑧选填序号),还需补充的仪器是_____。(填名称)
(2)若利用一种药品按照下图装置制取氧气,发生的反应方程式为_____。
(3)用排水法收集氧气,当观察到导管口_____时,开始收集,气体逸出的原因是由于试管内温度升高且_____,使试管内压强大于外界大气压,在压强差的作用下,气体逸出。
(4)将制取氧气过程中和检验氧气的装置图在图中补充完整_____。
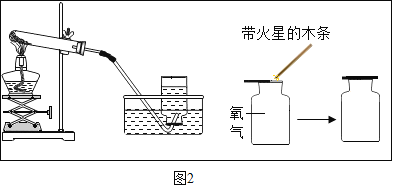
(5)用⑨装置收集O2时,气体应从_____。(“b”端或“c”端)通入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下充分反应后,测得有关数据如下表所示:
物质 | M | N | Q | P |
反应前质量/g | 4 | 10 | 1 | 21 |
反应后质量 /g | 0 | 12 | 15 | 待测 |
已知M的相对分子质量为n,P的相对分子质量为2n,下列推理正确的是 。
A.反应后生成Q的质量为15g
B.反应中N与P发生改变的质量之比为1∶1
C.反应后P的质量为12g
D.该反应化学方程式中M与P的化学计量数之比为2∶3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是某同学在探究金属活动性顺序时所做实验,通过实验现象不能得到的结论是 。
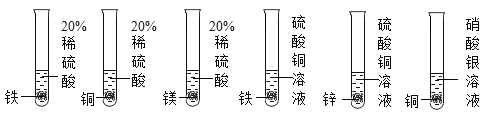
A.金属活动性由强到弱的顺序为镁、铁、铜
B.铁比铜活泼
C.铜能置换硝酸银溶液中的银
D.铜能置换出硝酸锌溶液中的锌
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学配制60g溶质质量分数为5%的NaCl溶液,准备了下列实验用品.回答下列问题:

(1)该同学按下列实验步骤进行:①计算,②称量,③量取,④________(填步骤名称).
(2)配制过程还缺少的一种玻璃仪器是__________(填名称).
(3)计算所需NaCl的质量___g,称量时,NaCl应放在托盘天平的__盘(填左、右)上.
(4)量取蒸馏水操作如下:将蒸馏水注入量筒,待液面接近量取体积对应刻度线时,改用_______(填仪器名称)滴加蒸馏水至刻度线.
(5)若用俯视的方式量取水的体积,所配制溶液的溶质质量分数会______(填“偏大”、“偏小”或“无影响”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组的同学利用下图装置,探究化学反应前后物质的质量是否守恒。应选用的药品是
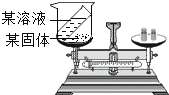
A.铁粉和稀盐酸液体中
B.硝酸钾晶体和水
C.碳酸钡粉末和稀硫酸
D.铜粉和硝酸银溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为某同学探究铁、铜、银三种金属活动性顺序的一组实验。
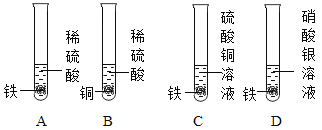
(1)上述实验中,有气泡产生的是_____。
(2)通过上述实验,还不能证明铁、铜、银三种金属的金属活动性顺序,请你在此基础上补充一个实验帮助这位同学达到实验目的(写出实验步骤、现象及结论)_____。
(3)某同学将一小包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液,并对滤液的组成进行探究。同学们对滤液中所含的溶质做出多种猜想,其中有两种猜想可能成立,这两种猜想是:(以下填写滤液中物质的化学式(水除外))①_____②_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动。
(探究活动一)试验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因:_____。
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
实验步骤 | 实验现象 | 实验结论 |
取氢氧化钙样品少量,研细后加适量蒸馏水充分混合后静置,_____ | _____ | 该样品还含有氢氧化钙 |
(探究活动二)测定样品中含有的变质固体(以下用 R 表示)的质量分数取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数。实验装置(气密性良好)如图 1 所示。
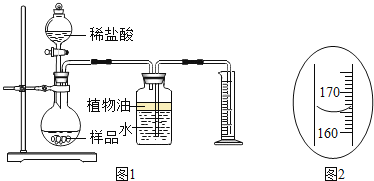
(3)将稀盐酸滴入样品中,产生气体的化学方程式为_____,反应一段后, 当观察到_____(填实验现象),才停止滴加稀盐酸。
(4)实验中量筒的作用是_____。
(5)实验结束后,量筒内进入水的体积如图 2 所示,其读数为_____mL。已知在该实验条件下,生成气体的密度为 2 g·![]() ,通过计算,样品中R的质量分数为_____。
,通过计算,样品中R的质量分数为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com