
| 金属 | Cr | Al | Cu |
| 与硫酸反应现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
分析 (1)根据金属的性质,分析实验前进行打磨的目的;
(2)根据实验一的现象及探究结果;
(3)根据验证三种金属活动性的方案设计思路,分析实验方案不可行的原因;
(4)根据所探究的三种金属的活动性,可以借助“三选中”的设计思路,另行设计检验三种金属活动性的方案,写出所需要的药品;
(5)总结比较金属活动性的实验方案.
解答 解:(1)由于金属在保存时可能与空气中氧气发生氧化,使表面形成氧化层,影响实验,因此要使用砂纸进行打磨;
(2)同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀硫酸中反应,Cr反应缓慢,Al反应剧烈,Cu无明显现象,说明金属的活动性Al>Cr>Cu;
(3)若使用硫酸铜溶液代替稀硫酸,由于铬、铝都能置换出铜而无法检验铬与铝的活动性强弱,因此不宜使用硫酸铜溶液代替稀硫酸;
(4)根据三种金属的活动性顺序Al、Cr、Cu,据“三选中”的设计思路,可选取金属铝、铜分别放入硫酸亚铬溶液中或把金属铬分别放入硫酸铝、硫酸铜溶液中进行三种金属活动性的检验;
(5)利用金属与酸发生置换反应或金属与盐反应置换反应都可以检验金属的活动性;
故答案为:
(1)除去金属表面氧化物(或污物);
(2)小雷;
(3)无法比较铬和铝的金属活动性强弱;
(4)A1、CrSO4溶液、Cu;
(5)金属与酸发生置换反应;金属与盐发生置换反应.
点评 验证三种金属活动性强弱关系时,通常采取“三取中”即:取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.


科目:初中化学 来源:山东省临沂市2017届九年级中考模拟八化学试卷 题型:选择填充题
如图所示是甲、乙、丙三种物质的溶解度曲线图,下列相关说法中不正确的是( )
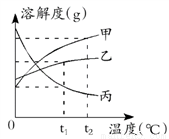
A. 甲、乙、丙三种物质的溶解度都随温度升高而增大
B. t2℃时,甲溶液的溶解度最大,丙的溶解度最小
C. 将t1℃时的丙的饱和溶液升温至t2℃,溶质的质量分数减小
D. 将t2℃时的甲的不饱和溶液降温,有可能会得到它的饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
A | B | C | D | |
| A | / | ↓ | ↑ | ↓ |
| B | ↓ | / | - | ↓ |
| C | ↑ | - | / | ↓ |
| D | ↓ | ↓ | ↓ | / |
| A. | 纯碱溶液.稀盐酸.硝酸银溶液.氯化钡溶液 | |
| B. | 纯碱溶液.氯化钡溶液.稀盐酸.硝酸银溶液 | |
| C. | 稀盐酸.纯碱溶液.硝酸银溶液.氯化钡溶液 | |
| D. | 稀盐酸.纯碱溶液.氯化钡溶液.硝酸银溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷燃烧发光放热,发出黄白色火焰,产生浓厚白烟,生成五氧化二磷固体 | |
| B. | 镁在空气中燃烧:发出强光,放出热量,产生大量的白雾 | |
| C. | 向硫酸铜溶液中加入铁钉:铁钉表面覆盖一层白色物质,溶液变成浅绿色 | |
| D. | 硫在氧气中燃烧,发出明亮的蓝紫色火焰,放热,生成有刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某石灰石中含有杂质(杂质不溶于水,也不与盐酸反应),一兴趣小组想测定该样品中碳酸钙的质量分数,他们将一块样品敲打粉碎后,称出6g放入质量为20g的烧杯中,然后加入50g稀盐酸,用玻璃棒搅拌至不再产生气泡(盐酸有剩余),反应所需时间和烧杯及其所盛物质的总质量变化如图所示图:
某石灰石中含有杂质(杂质不溶于水,也不与盐酸反应),一兴趣小组想测定该样品中碳酸钙的质量分数,他们将一块样品敲打粉碎后,称出6g放入质量为20g的烧杯中,然后加入50g稀盐酸,用玻璃棒搅拌至不再产生气泡(盐酸有剩余),反应所需时间和烧杯及其所盛物质的总质量变化如图所示图:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | B | C | D | |
| 区分的 物质 | 生铁和钢 | 饱和与不饱和的硝酸钾溶液 | 硬水和软水 | 氧气和二氧化碳 |
| 方案一 | 取样,分别加入硫酸铜溶液 | 升高温度 | 观察颜色 | 燃着的木条 |
| 方案二 | 分别用磁铁吸引 | 加入少量的硝酸钾固体 | 加肥皂水 | 澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 反应前 | 反应后 | ||
| 实验 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和混合物的质量 |
| 数据 | 120g | 11g | 126.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
| 元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
| 原子结构示意图 | 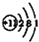 | 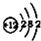 | 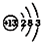 | 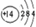 | 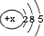 | 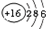 | 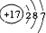 | 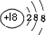 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com