
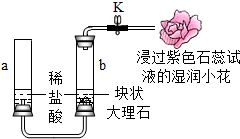
 某实验小组用如图装置研究CO2的性质.提示:
某实验小组用如图装置研究CO2的性质.提示:

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:初中化学 来源: 题型:

| 序号 | t/h | t/℃ | m/g | x |
| 1 | 3 | 80 | 5 | 4 |
| 2 | 3 | 160 | 10 | 1 |
| 3 | 4 | 160 | 10 | 0.8 |
| 4 | 4 | 160 | 5 | 0 |
| 5 | 5 | 80 | 5 | 3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
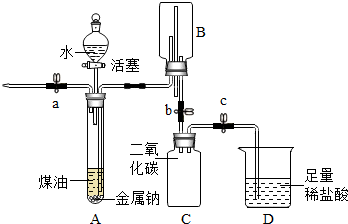 在金属活动性顺序里,钠位于铜之前.某化学兴趣小组发现,将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,却未置换出红色的铜.该小组同学对此现象进行了如下探究:
在金属活动性顺序里,钠位于铜之前.某化学兴趣小组发现,将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,却未置换出红色的铜.该小组同学对此现象进行了如下探究:| 实验操作 | 实验现象及分析 | |
| ① | 打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞. | 实验现象为:液体分层,钠熔成银白色小球,在液体分层的界面上跳动,产生大量气泡,下层液体逐渐被压入B中. 钠的物理性质有: |
| ② | 打开止水夹b,待B中部分液体进入C中,迅速关闭止水夹b. | 发生反应的化学方程式为: |
| ③ | 打开止水夹c. | 实验现象为:D中液体 |
| ④ | 打开止水夹a,通过分液漏斗向大试管中逐滴加水,将燃着的木条伸至装置左端尖嘴导管口. | 实验现象为:气体燃烧,产生 |
| ⑤ | 在火焰上方罩一个干冷的烧杯. | 实验现象为:烧杯内壁出现 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
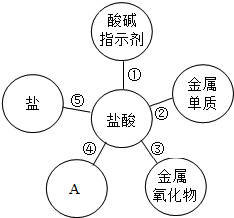 归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).
归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
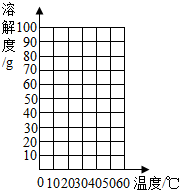 请根据你学习的有关溶液的知识,回答下列问题:
请根据你学习的有关溶液的知识,回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | A物质 | 30 | 35 | 45 | 50 |
| B物质 | 25 | 35 | 55 | 90 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com