
| A. | 若a=1,则b=2 | |
| B. | 反应后金属的质量不可能超过21.6克 | |
| C. | a+b不可能大于4 | |
| D. | 当得到的金属质量为20克时,a一定等于3 |
分析 在金属活动性顺序中只要排在前面的金属就能把排在后面的金属从其盐溶液中置换出来,由于金属的活动性Fe>Cu>Ag;用不同的金属置换同种盐溶液,盐中金属先被排在金属活动性顺序中较前的金属置换出来.另外,若有一种金属和多种混合盐溶液反应,最先反应的是最不活泼的那个金属的盐溶液.可以据此分析该题.
解答 解:由金属活动性顺序表可知,金属的活动性Fe>Cu>Ag,向AgNO3溶液中加入一定质量的Fe和Cu的混合粉末,Fe首先与硝酸银溶液反应,Fe反应完成时,Cu再与硝酸银反应.化学方程式为:①Fe+2AgNO3=2Ag+Fe(NO3)2;②Cu+2AgNO3=2Ag+Cu(NO3)2
A、当a=1时,则得到的金属为银,Cu和Fe全部反应,硝酸银溶液足量.恰好反应时,溶液中的溶质为硝酸铜和硝酸亚铁;硝酸银过量时,溶液中的溶质为硝酸铜、硝酸亚铁和硝酸银,因此,b=2或b=3;故A错误;
B、但上述两个反应恰好进行完全时,得到的金属的量最大,
设生成银的质量分别为x,y
Fe+2AgNO3=2Ag+Fe(NO3)2 Cu+2AgNO3=2Ag+Cu(NO3)2
56 216 64 216
5.6g x 6.4g y
$\frac{56}{5.6g}$=$\frac{216}{x}$ $\frac{64}{6.4g}$=$\frac{216}{y}$
x=21.6g y=21.6g
因此,反应后金属的质量不可能超过21.6g+21.6g=43.2g,
故B错误;
C、由A知,a=1时,b最大为3,a+b=4;当硝酸银极少时,①反应未进行完,Fe有剩余,则金属为Fe、Cu、Ag,溶液中的溶质为硝酸亚铁,a=3,b=1,a+b=4,故C正确;
D、当Fe恰好反应时,得到银为21.6g,当得到的金属质量为20克时,Fe有剩余,①反应未进行完,则金属为Fe、Cu、Ag,a=3,故D正确.
故选CD.
点评 主要考查了对金属的活动性顺序的应用和金属与盐反应时应该注意的事项,培养学生分析问题、解决问题的能力.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
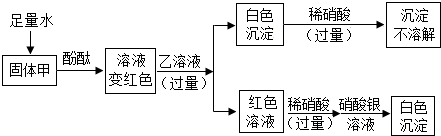
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
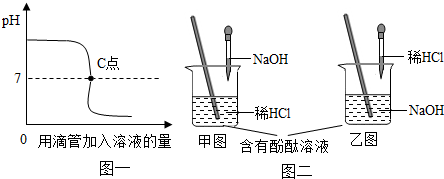
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷、水、碘酒、胆矾 | B. | 水银、干冰、熟石灰、石油 | ||
| C. | 液氧、生石灰、稀硫酸、空气 | D. | 石墨、氧化铜、粗盐、天然气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用10mL的量筒量取9.0mL水 | |
| B. | 用向下排空气法收集纯净的氢气 | |
| C. | 将氯化钠的溶液蒸发时待蒸发皿有少量晶体出现即可停止加热 | |
| D. | 用托盘天平称取10.58g碳酸钠粉末 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | d1>d2 | B. | d1<d2 | C. | d1=d2 | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com