
【题目】黄铜是铜和锌的合金,某化学兴趣小组为研究合金中铜的含量,取样品 15g进行如下操作。
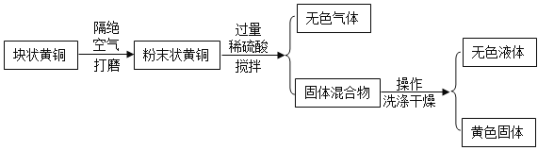
(1)操作①的名称是_____。该操作用到的玻璃仪器有玻璃棒、烧杯、_____。
(2)加入稀硫酸发生的反应的化学方程式为_____。
(3)最后称得黄色固体为 13g,得到含铜量为 86.7%,高于实际含铜量,其原因可能是_____。
【答案】过滤 漏斗 Zn+H2SO4═ZnSO4+H2↑ 由于铜覆盖在锌的表面,使锌不能完全参加反应(或黄铜没有研磨得足够细,使部分锌没有参加反应)
【解析】
(1)根据过滤的原理和操作分析回答;
(2)根据锌能与稀硫酸反应写出反应的化学方程式;
(3)根据生成的铜覆盖在锌的表面分析回答。
(1)操作①能将固液分开,名称是过滤,该操作用到的玻璃仪器有玻璃棒、烧杯、漏斗。故填:过滤,漏斗。
(2)加入稀硫酸发生的反应的是锌与稀硫酸反应生成了硫酸锌和氢气,化学方程式为:Zn+H2SO4═ZnSO4+H2↑,故填:Zn+H2SO4═ZnSO4+H2↑。
(3)最后称得黄色固体为13g,得到含铜量为86.7%,高于实际含铜量,其原因可能是:由于铜覆盖在锌的表面,使锌不能完全反应(或黄铜没有研磨得足够细,使部分锌没有参加反应)。故填:由于铜覆盖在锌的表面,使锌不能完全参加反应(或黄铜没有研磨得足够细,使部分锌没有参加反应)。


科目:初中化学 来源: 题型:
【题目】实验课上,某小组的同学用块状生石灰进行“化学反应中能量的变化”实验时发现:向块状生石灰样品中加入适量水后没有明显的温度变化。为确定其原因,进行了如下实验探究。实验验证一。
[提出问题]生石灰是否变质?其成分是什么?
[查阅资料]氢氧化钙溶解过程中无明显温度变化,与盐酸反应无气体生成。
[猜想与假设]同学们认为块状生石灰样品已变质,并对其成分作出了如下4种猜想。
猜想1:氧化钙和氢氧化钙:猜想2:氧化钙和碳酸钙:猜想3:______________;
猜想4:氧化钙、氢氧化钙和碳酸钙。
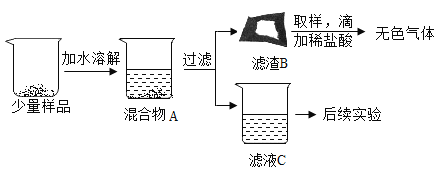
[进行实验]同学们将少量样品研碎后,按如图所示过程进行实验。
(1)在溶解过程中用温度计测量液体的温度,发现温度计示数升高,说明样品中应该含有______________。
[结论]猜想3不成立。
(2)滤渣B中一定含有_____________,用化学方程式表示变质过程中生成该物质的反应_____________。
[结论]①块状生石灰表面发生变质:②猜想1不成立。
(3)为验证滤液C的成分,进行后续实验。
实验操作 | 实验现象 | 实验结论 |
____________ | ____________ | ② 滤液中溶质为氢氧化钙 ②猜想4成立,猜想2不成立 |
[反思与评价]
(4)有的同学认为上述实验过程不能得出猜想4成立、猜想2不成立的结论,理由是______________。
[注意:答对15题以下小题奖励4分,化学试卷总不超过60分]
实验验证二:为了进一步确定块状生石灰样品的成分及质量,实验小组利用如下图所示的装置(夹持仪器省略)进行实验。
查阅资料:氢氧化钙加热至580°C、碳酸钙加热至825°C分别分解生成两种氧化物。
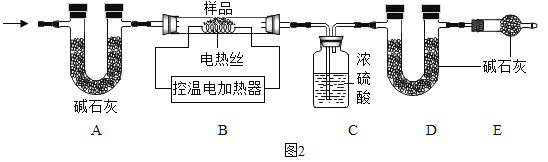
(5)①装置E的作用是______________。
②控温电加热器使装置B中反应完全,再通一段时间空气,测得反应前后装置C、D分别增重18.0g和22.0g,将装置B中反应后剩余的固体氧化物加入足量水中溶解,蒸发所得固体(不含水)增重36. 0g.求原块状生石灰固体样品中各成分为______________,各物质的质量______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图所示是实验室制取气体的部分装置,请回答下列问题:
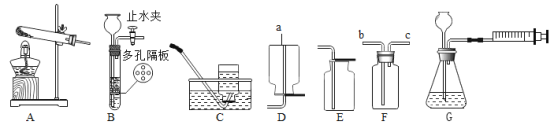
(1)写出仪器a的名称_____。
(2)小丁同学用装置B制取CO2,请写出该原理的化学方程式:_____。
(3)采用装置F,用排水法收集氧气,气体从_____(填“b”或“c”)端进。
(4)要检查G 装置的气密性,其操作及现象是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是几种实验室制取气体的发生装置和收集装置,请回答下列问题:
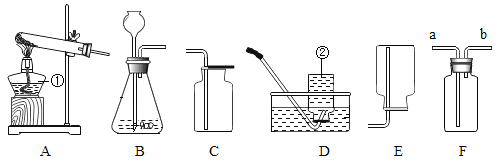
(1)指出图中标有数字的仪器名称:①_____。
(2)写出实验室用双氧水和二氧化锰制取氧气的化学方程式_____;要制取较为纯净的氧气时装置组合应选用_____(填字母标号,下同)。
(3)若将F装置内装满水,再连接量筒,用可用于测定不溶于水且不与水反应的气体体积,测量时气体应从_____,(填“a”或“b” )进入F中。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】BaCl2是一种重金属盐,其水溶液具有很强的毒性。若误服了BaCl2溶液可立即服用MgSO4溶液解毒。为测定某BaCl2溶液的溶质质量分数,现取100克BaCl2溶液,不断加入MgSO4溶液,反应过程中溶液总质量与加入MgSO4溶液的质量关系如图所示,请回答:
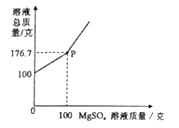
(1)P点时溶液中的溶质名称是 ;
(2)反应生成沉淀的最大质量为 克;
(3)求原BaCl2溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知反应前后有元素化合价改变的反应统称为氧化—还原反应,如图为反应类型的关系图,下列有关说法正确的是 ( )
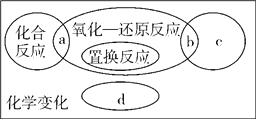
A. CO2+H2O=== H2CO3属于a处的反应
B. 2H2O![]() 2H2↑+O2↑属于氧化—还原反应
2H2↑+O2↑属于氧化—还原反应
C. c处反应后物质的质量一定减小,不符合质量守恒定律
D. 任何两种化合物之间发生反应都属于d
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组设计了一组实验,己知甲中盛有一定量的碳酸钠溶液,实验流程如图所示:下列说法正确的个数是
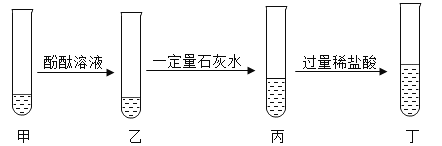
①乙中溶液为红色
②丙中溶液的溶质组成有2种可能情况
③丙中加入过量稀盐酸后,观察到的现象为有气泡产生,溶液由红色变为无色,白色沉淀消失
④丁中溶液的溶质除酚酞外,只有氯化钠、氯化氢
A.1
B.2
C.3
D.4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们在初中化学实验室中,发现一瓶如图所示久置的无色溶液,瓶口有白色固体、瓶塞丢失,已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定原溶液成分,同学们进行了如下探究:
![]()
(1)小张同学取待测液测得pH=10,他得出的关于溶液成分的结论是_____。他取少量待测液于试管中,加入过量的稀HCl,看到_____,由此小张同学认为该溶液为Na2CO3溶液。
(2)小李同学对小张同学的结论提出疑问,由此进行了以下实验:取少量待测液于试管中,加入过量的CaCl2溶液,生成白色沉淀,该反应方程式为_____,静置,(写出还需进行的操作及现象)_____。
通过实验,小李认为小张结论正确。
二位同学给试剂瓶贴一新标签:Na2CO3。
(3)实验结束后,同学们通过讨论认为试剂瓶原标签仍有可能不是Na2CO3,你猜测他们认为该试剂瓶原标签上的化学式可能是_____;你的理由是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com