
【题目】程浩同学查阅资料得知:Cu 与稀硫酸不反应,但Cu可与浓硫酸在加热的条件下反应,化学方程式为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2R,下列说法中不正确的是
CuSO4+SO2↑+2R,下列说法中不正确的是
A. 该反应中涉及了3种类型的化合物
B. R为相对分子质量最小的氧化物
C. 反应前后,H2SO4中硫的化合价全部发生了改变
D. 该反应不属于四种基本反应类型中的任何一种
【答案】C
【解析】
根据反应的化学方程式Cu+2H2SO4(浓)![]() CuSO4+2R+SO2↑,反应物中铜、氢、硫、氧原子个数分别为1、4、2、8,反应后的生成物中铜、氢、硫、氧原子个数分别为1、0、2、6,根据反应前后原子种类、数目不变,则2R中含有4个氢原子和2个氧原子,则每个R分子由2个氢原子和1个氧原子构成,物质R的化学式为H2O。
CuSO4+2R+SO2↑,反应物中铜、氢、硫、氧原子个数分别为1、4、2、8,反应后的生成物中铜、氢、硫、氧原子个数分别为1、0、2、6,根据反应前后原子种类、数目不变,则2R中含有4个氢原子和2个氧原子,则每个R分子由2个氢原子和1个氧原子构成,物质R的化学式为H2O。
A、H2SO4属于酸,CuSO4属于盐,SO2、H2O属于氧化物,该反应中涉及了3种类型的化合物,故A正确;
B、R的化学式为H2O,H2O为相对分子质量最小的氧化物,故B正确;
C、硫酸中部分硫元素的化合价由+6价变为+4价,部分硫元素的化合价不变,故C错误;
D、该反应的反应物是两种,反应物是三种,不属于四种基本反应类型中的任何一种,故D正确。故选C。


科目:初中化学 来源: 题型:
【题目】试依据核电荷数为1--18的元素的原子结构示意图,回答下列问题:
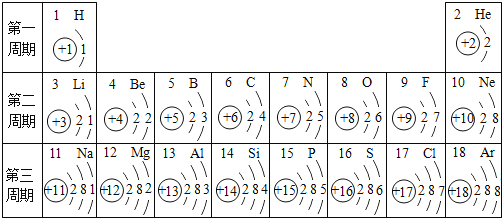
(1)图中硫元素与氮元素属于不同种元素的原因是_____不同;硫元素的化学性质与氧元素的化学性质______。
(3)核电荷数为12的元素的原子失去两个电子后,形成的粒子的符号是______.它的核外电子排布与______的原子核外电子排布相同。
(4)钙元素是人体中的常量元素,它在人体内99%存在于骨骼和牙齿中.该元素的原子序数为_____,该元素在周期表中位于第____周期。
(5)月球上的3He(3表示相对原子质量)蕴藏量巨大,探月的目标之一是探测核聚变燃料3He的分布.地球上的氦元素主要以4He形式存在,从原子的构成来看,3He、4He两种原子的电子数_______(填“相同”或“不同”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一定条件下下列反应都能发生,其中既属于化合反应又属于氧化反应的是( )
A.葡萄糖+氧气![]() 水+二氧化碳
水+二氧化碳
B.高锰酸钾![]() 锰酸钾+二氧化锰+氧气
锰酸钾+二氧化锰+氧气
C.镁+氧气![]() 氧化镁
氧化镁
D.氨气+氯化氢![]() 氯化铵
氯化铵
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文(原文作者:段翰英等)。
我国制作泡菜的历史悠久。制作泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成。泡菜品种繁多、风味独特、口感鲜脆。
蔬菜中含有硝酸盐。硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。亚硝酸盐[如亚硝酸钠(![]() )]与胃酸(主要成分是盐酸)反应,产生亚硝酸(
)]与胃酸(主要成分是盐酸)反应,产生亚硝酸(![]() )和氯化物(如
)和氯化物(如![]() )。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
泡菜中含亚硝酸盐吗?含量有多少?含量受什么因素影响呢?
经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。

用不同的蔬菜进行测定,变化趋势与芹菜相似。
实验表明,发酵温度对泡菜中亚硝酸盐的生成量及生成时间也具有明显的影响。泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现的早,且数值低。这与温度较高有利于乳酸菌的繁殖有关。
实验还表明,泡制过程中添加姜汁和维生素C,都能有效地减少亚硝酸盐的生成。
现代医学证明,泡菜中的乳酸和乳酸菌对人体健康有益,具有抑制肠道中的腐败菌生长、降低胆固醇等保健作用。但是,有些泡菜盐分或糖分过高,对高血压和糖尿病等慢性病患者不利。另外,泡制过程也会造成某些营养素的流失。(有删改)
依据文章内容,回答下列问题。
(1)泡菜中的亚硝酸盐是由__________转化生成的。
(2)室温下,用芹菜制作的泡菜,最佳食用时间是__________(填字母序号,下同)。
A.泡制2-3天 B.泡制5-6天 C.泡制12天后
(3)下列关于制作泡菜的说法中,合理的是__________。
A.最好加入一些姜汁 B.最好在较低温度下泡制
C.最好加入一些富含维生素C的水果
D.最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关
(4)请你为喜欢吃泡菜的人提一条食用泡菜的建议:__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钼是稀有矿产资源,主要用于航天合金材料制作。在元素周期表中钼元素的某些信息如图所示,下列有关钼的说法正确的是
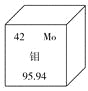
A. 原子核内质子数为42
B. 相对原子质量为95.94g
C. 属于非金属元素
D. 元素符号为MO
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向100 g CuSO4与H2SO4的混合溶液中加入质量分数为20%的氢氧化钠溶液,产生沉淀的质量与所加氢氧化钠溶液的质量关系如图所示,回答下列问题:

(1)由图像可知,NaOH先与混合溶液中 发生反应。
(2)生成沉淀Cu(OH)2的质量是多少?
(3)当加入NaOH溶液的质量为40 g时,所得溶液中Na2SO4的质量分数是多少?(结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,三个实验操作都是错误的,请根据要求作简要回答.
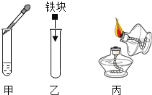
![]() 图甲的错误之处是________.
图甲的错误之处是________.
![]() 图乙的错误操作可能产生的后果是________;
图乙的错误操作可能产生的后果是________;
![]() 图丙的错误造成的后果是________.
图丙的错误造成的后果是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析推理是化学学习中常用的思维方法。下列分析推理正确的是( )
A.水分子是由氢原子和氧原子构成的,所以氢原子和氧原子能保持水的化学性质
B.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
C.单质含有一种元素,所以含有一种元素的纯净物一定是单质
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组对“氧化铜能否作过氧化氢分解的催化剂“进行了探究
(实验探究)
实验编号 | 实验操作 | 实验现象 | 实验分析或结论 | |
实验分析 | 实验结论 | |||
① |
| 有少量气泡;木条不复燃 | 过氧化氢能分解,但是 _________ | 氧化铜是过氧化氢分解的催化剂 |
② |
| __________________ | 氧化铜能加快过氧化氢分解 | |
(1)写出实验②中反应的化学方程式:___________________。
(交流反思)实验过程中加入到两支试管里的过氧化氢溶液应满足的要求有_________________。
①体积相同 ②浓度相同 ③温度相同
(2)小明同学认为仅由上述实验还不能完全得出表内的“总结”,他补充设计了以下两个探究实验
实验一:称量反应后固体质量,并与反应前的称量数据作比较,其目的是________________。
实验二:另取5mL5%的过氧化氢溶液于试管中,再向其中加入实验②反应后的固体剩余物,如图1所示,其目的是证明_______________________。
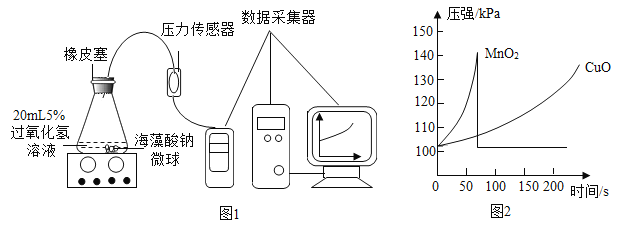
(实验拓展)小红同学用MnO2、CuO两种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球探究分解过氧化氢溶液制取氧气的适宜催化剂。
实验操作:取30粒含MnO2的海藻酸钠微球,采用图1装置进行实验。改用另一种微球,分别重复上述实验,得到图2的锥形瓶内压强随时间变化的曲线图。
(3)每次实验时,海藻酸钠微球数应相同的原因是_____________。
(4)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是_______________。
(5)从实验曲线看,催化效果较好、反应温和的催化剂是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com