
分析 (1)根据化肥所提供作物生成元素把化肥分为:提供N元素的氮肥,提供P元素的磷肥,提供K元素的钾肥,提供N、P、K三种中两种或以上元素的复合肥;根据“碳铵”(NH4HCO3)的化学式确定碳铵为氮肥;由于碳酸在常温下就能分解且温度越高分解越快,可判断碳铵化学性质不稳定,保存时应避免曝晒;由于铵根遇碱释放出氨气而降低肥效,保存要应避免与碱性物质共存;
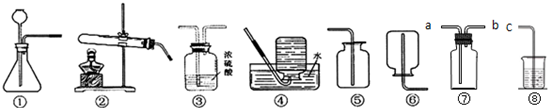
(2)装置②适用于对固体加热产生气体的反应,进行“碳铵”固体受热分解的实验宜采用该装置;碳铵受热时发生分解反应,可生成氨气、水和二氧化碳;实验室通过采取加热高锰酸钾或氯酸钾制取氧气,在加热固体高锰酸钾或氯酸钾制氧气时也可采取装置②;
(3)装置①适用于固体与液体常温下反应制取气体,因此,利用碳酸钙与盐酸、锌与硫酸、过氧化氢与二氧化锰制取二氧化碳、氢气、氧气时可选用该装置;在收集气体时,氧气、二氧化碳密度比空气的大可选择⑤向上排空气法收集,氢气密度小于空气可选择⑥向下排空气法收集,氧气、氢气难溶于水可选择④排水法收集;
(4)①酚酞试液变红,说明氨水呈碱性,碱性溶液pH大于7;
②装置③内盛放浓硫酸,浓硫酸可与氨气反应生成硫酸铵,不能用于干燥氨气;
③氨气密度小于空气应排取向下支收集,因此,采取装置⑦收集氨气时,氨气应从b管进入使瓶内空气由下部的a管排出;氨气极易溶于水或与酸溶液发生反应,因此可在烧杯内放水或酸溶液吸收多余的氨气.
解答 解:(1)根据“碳铵”(NH4HCO3)的化学式可知碳铵可提供作物生成所需的N元素,因此应属于氮肥;
由于碳酸在常温下就能分解且温度越高分解越快,因此推断碳铵化学性质不稳定;
碳铵化学性质不稳定且易潮解,因此在保存、运输时应密封,不要受潮和曝晒等;“碳铵”遇碱放出氨气,在保存时不能与碱性一起存放;
故答案为:氮;不稳定;①②;
(2)进行“碳铵”固体受热分解的实验需要选择适用于加热固体制取气体的装置②;加热过程中,碳铵受热分解生成氨气、水和二氧化碳;该装置还可用于高锰酸钾受热分解制取氧气;
故答案为:②;NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O;实验室用高锰酸钾加热制取氧气;
(3)装置①适用于固体与液体常温下反应制取气体,因此,利用固体碳酸钙与盐酸溶液制取二氧化碳时可选用该装置;在收集气体时,二氧化碳密度比空气的大可选择⑤向上排空气法收集,二氧化碳能溶于水不可选择④排水法收集;
故答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O;⑤;
(4)①产生的氨气缓缓通入盛有酚酞试液的试管中,酚酞试液变红,证明氨水呈碱性,其溶液pH大于7;
故答案为:碱;>;
②氨气能与浓硫酸反应生成硫酸铵而被干燥剂浓硫酸吸收,因此,不能使用浓硫酸干燥氨气;
故答案为:不能,因为氨气能与浓硫酸发生化学反应而被吸收;
③氨气密度小于空气应排取向下支收集,采取装置⑦收集氨气时,氨气应从b管进入使瓶内空气由下部的a管排出;因此,应将a管与c进行连接;为吸收多余的氨气,可在烧杯内放水或酸溶液;
故答案为:a;水或某种酸液.
点评 浓硫酸为酸性干燥剂,只能用于干燥遇水呈酸性的二氧化碳、或遇水呈中性的氢气和氧气等气体;而干燥遇水呈碱性的氨气时,只能选择碱性干燥剂氢氧化钠、碱石灰等,或中性干燥氯化钙等.


 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:初中化学 来源: 题型:实验探究题
| 方案 | 药品 | 实验现象 | 结论 | 反应原理(即方程式) |
| 方案 (取样) | 紫色石蕊试液 | 一支试管中溶液颜色变红色,一支试管溶液颜色变蓝色 | 能使紫色石蕊试液变红色的是稀盐酸,变蓝色的是氢氧化钠溶液 | 紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只有①④ | B. | ①②④ | C. | ①③④ | D. | 只有②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe和Cu | B. | Fe和Ag | C. | Ag | D. | Cu 和Ag |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
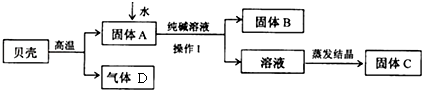
| 实验操作 | 现象 | 结论 | |
| 甲 | 取少量固体C,溶于适量水形成溶液后,滴加几滴酚酞试液 | 溶液变红 | 猜想成立 |
| 乙 | 取少量固体C,溶于适量水形成溶液后,滴加足量稀硫酸 | 无气泡产生 | 猜想不成立 |
| 丙 | 取少量固体C,溶于适量水形成溶液后,滴加几滴饱和碳酸钠溶液 | 出现白色沉淀 | 猜想成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
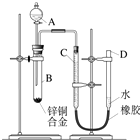 某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数.
某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com