
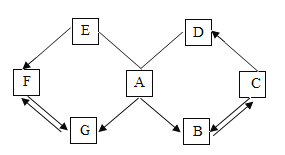
【题目】已知 A、B、C、D、E、F、G 是初中化学常见的物质,它们存 在如图所示的关系,图中“→”表示可以向箭头所指的方向一步转化,“— 表示两种物质之间能相互反应(反应条件、部分物质已略去)。已知 A 是 人体胃液中含有的酸,C 可改良酸性土壤,A、B、C、D、E 为五种不 同类别的物质,E、F、G 物质类别相同,请回答下列问题
(1)写出 A 的化学式:_____。
(2)写出 F→G 的化学方程式:_____。
【答案】HCl Fe+H2SO4===FeSO4+H2↑或Fe+2HCl===FeCl2+H2↑
【解析】
已知 A 是人体胃液中含有的酸,则A是盐酸,C 可改良酸性土壤,则C是氢氧化钙;A、B、C、D、E 为五种不同类别的物质,那么B、D、E不可能是酸或碱,可能是盐、氧化物或单质。而A、C都能生成B,则B可能是氯化钙或水,但氯化钙不能一步转化为氢氧化钙,所以B为水,水和氧化钙能生成氢氧化钙;C可以生成D,A与D能反应,则D为盐类,所以D为碳酸钙,碳酸钙与盐酸能反应,且氢氧化钙与二氧化碳能生成碳酸钙;根据物质类别E剩余应该为单质, E、F、G 物质类别相同,则G也是单质,盐酸能生成单质G,那么G为氢气;单质F也能生成氢气,则F为较活泼金属单质,E能与盐酸反应,则E也是较活泼金属单质,E生成F,则E的金属活动性要强于F的金属活动性,那么E可以为锌,F可以为铁。
(1)A是人体胃液中含有的盐酸,化学式为HCl。
(2)F→G是铁与稀酸反应生成盐和氢气,化学方程式为:Fe+H2SO4===FeSO4+H2↑或Fe+2HCl===FeCl2+H2↑


科目:初中化学 来源: 题型:
【题目】在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如图所示。下列叙述中不正确的是( )

C是空气中体积分数最大的物质
B.A的水溶液能使无色的酚酞试液变红
C.在该反应中,生成C和D的质量比为14∶9
D.该反应的基本反应类型为置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下图提供的装置和试剂,组装一套用一氧化碳使氧化铜还原成铜的实验装置,并回答下列问题。
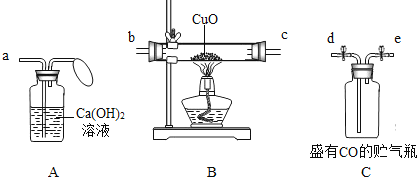
(1)实验时气体按图示从左向右流动,则这套装置的连接顺序是(填接口处字母): ___接___,__接___。
(2)实验开始时是先加热氧化铜,还是先通入CO? ___,理由是_______。写出装置B中发生反应的化学方程式________。
(3)装置A的作用是①__;②___。写出装置A中发生反应的化学方程式___。
(4)实验后怎样处理气球里的尾气? ____。
(5)贮存在装置C中的CO是先在贮气瓶中注满水,然后用排水法收集的。贮气时CO应从__通入贮气瓶中(填接口处字母)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组在制取氧气的实验过程中,有如下实验设计方案,该方案的实验目的是:探究_______对反应速率的影响。
编号 | 温度 | 催化剂 | 氯酸钾、二氧化锰的质量比 | 生成1升氧气所需时间/s |
实验Ⅰ | 400℃ | MnO2 | 1:1 | 153 |
实验Ⅱ | 400℃ | MnO2 | 2:1 | 240 |
小芳在实验时,误把氧化铁当作二氧化锰放入加热,结果发现也能较快产生氧气,于是进行如下探究:
(猜想Ⅰ)除二氧化锰、氧化铜外,氧化铁(Fe2O3)也可以作氯酸钾分解的催化剂。
(设计实验)
按下表进行实验,并测定开始产生气体时的温度(提示:开始产生气体的温度越低,表示反应速度越快)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾和二氧化锰(质量比1︰1) | 350 |
③ | 氯酸钾和氧化铜(质量比1︰1) | 370 |
④ | 氯酸钾和氧化铁(质量比1︰1) | 390 |
(数据和结论)
(1)由实验_________与实验④对比,证明猜想合理;
(2)实验所用的三种物质中,催化效果最好的是__________。
(反思)
(1)若要证明氧化铁是该反应的催化剂,还需验证它在化学反应前后的______和______是否改变。小林在实验时,联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,提出猜想Ⅱ。
(猜想Ⅱ)过氧化钙与水反应可制取氧气。
实验装置 | 实验主要过程 |
| ①检查装置气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出。 |
实验结论:过氧化钙与水反应________(填“能”或“不能”)用于实验室制取氧气。
(分析与反思)
(1)过氧化钙与水反应虽然没有快速收集到大量氧气,但由此实验现象,小林认为渔民用过氧化钙做增氧剂的主要原因是__________。
(2)小林希望对此实验进行改进,使该反应加快,请你帮他提出合理化建议_________。
(3)同学们对过氧化钙与水反应的生成物猜想如下:①氢氧化钙和氧气②碳酸钙和氧气。你认为猜想_________ (填序号)一定是错误的,理由是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是硫和铁在空气和氧气中燃烧的实验。铁丝在空气中不能燃烧,但是纳米铁粉在空气中稍加热即可剧烈燃烧。下列说法正确的是( )
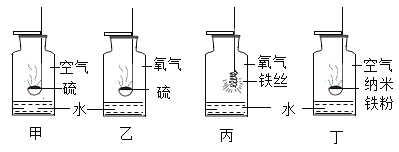
A.实验甲中观察到燃烧发出蓝紫色火焰,实验乙中观察到燃烧发出淡蓝色火焰
B.实验甲和实验乙中生成物相同,但是实验丙和实验丁的生成物不同
C.从四个实验中可以看出增大反应物的浓度和反应物接触面可以使反应更充分更剧烈
D.四个实验中水的主要作用是防止集气瓶炸裂
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料 甲醇,反应的微观示意图如下:
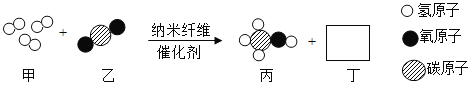
下列说法不正确的是
A.该反应是置换反应B.甲醇的化学式为 CH4O
C.乙是由分子构成的D.参加反应的甲和 CO2分子个数比为3:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】牙膏是常见的日用化学品,其中的摩擦剂可以增强牙膏对牙齿的摩擦作用和去污效果。已知某品牌牙膏的摩擦剂含有CaCO3 和SiO2,SiO2 不与稀盐酸反应。 现将 10 g 该摩擦剂加入到盛有足量稀盐酸的烧杯中,充分反应后,烧杯内物质的总 质量减少了 3.52 g。请计算:
(1)CaCO3 中钙元素与氧元素的质量比_____________。
(2)10 g 该摩擦剂中 CaCO3 的质量_____________。
(3)该摩擦剂中 SiO2 的质量分数_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钠是一种活泼金属,常温下能与氧气、水等物质发生反应。钠与水反应的化学方程式为:2Na+2H2O==2NaOH+H2↑。在实验室,小亮先取定量的硫酸铜溶液于烧杯中,再取一小块钠投入硫酸铜溶液中,充分反应后过滤,得到滤液和蓝色滤渣,并对滤被的成分进行探究。
(提出问题)滤液中溶质的成分是什么?
(查阅资料)Na2SO4溶液呈中性
(猜想与假设)猜想一:Na2SO4
猜想二:Na2SO4和NaOH
猜想三:____________
猜想四:Na2SO4、CuSO4和NaOH
小明认为猜想______不合理,理由是_______(用化学方程式表示)。
(实验与验证)
实验 | 实验操作 | 实验現象 | 实验结论 |
实验一 | 取少量滤液于试管中,仔细观察现象 | 溶液为无色 | 猜想_____不成立 |
实验二 | 向实验一所取滤液中滴入酚酞溶液 | ________ | 猜想二不成立 |
实验三 | 常温下,再取少量滤液,测溶液酸碱度 | pH=7 | 猜想_____成立 |
(拓展延伸)金属活动性顺序表中钠及前面的金属____(填“能”或“不能”)把位于后面的金属从它们盐溶液里置换出来。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学学习小组进行“铝和酸溶液反应的探究”的活动。用铝片分别和氢离子浓度相同的稀盐酸、稀硫酸反应,发现铝片和稀盐酸反应现象非常明显,而和稀硫酸却几乎不反应。
(提出问题)是什么原因导致两者的差异?
两种酸中氢离子浓度相同,那么存在的差异就可能跟H+所处的环境不同有关(如阴离子的不同)。
(作出猜想)猜想一:Cl-能促进金属铝与H+的反应。
猜想二:_____。
猜想三:铝表面的致密氧化膜有保护作用,使H+与铝不易接触。
为了验证上述假设,经充分讨论,大家设计了如下实验方案进行验证。
(查阅资料)已知 9.8%H2SO4 溶液和 7.3%HCl 溶液中 H+浓度相同。
(设计实验)
① | 9.8%H2SO4溶液5mL+铝片 | 不加其他试剂(对比) | 无气泡 |
② | 9.8%H2SO4溶液5mL+铝片 | 加入_____溶液 | 有较多气泡 |
③ | 9.8%H2SO4溶液5mL+铝片 | 加入 0.5mL Na2SO4 溶液 | 无气泡 |
④ | 7.3%HCl 溶液 5mL+铝片 | 加入_____溶液 | 有较多气泡 |
⑤ | 7.3%HCl 溶液 5mL+铝片 | 不加其他试剂(对比) | 有较多气泡 |
由实验②③得出猜想_____成立;由④⑤得出猜想_____不成立。为了验证猜想一成立,小明认为只需要在 5mL 9.8%H2SO4 溶液和铝片中加入_____,并与实验①对比即可。
(实验拓展)对于有气体生成的化学反应,我们可以用产生气体的速率来比较反应速率。为准确比较,应该测量收集相同体积气体所需的_____,因此,上述收集氢气应该采用_____法。
为了真实地观察未打磨的铝片与稀盐酸反应的情况,小红用压强传感器测量集气瓶中气体压强的变化,如图所示。
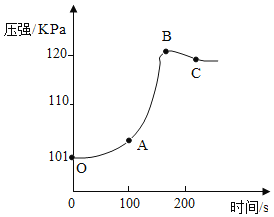
请解释曲线变化的原因:
OA 段_____;AB 段_____;BC 段_____。指出反应结束并恢复到常温时集气瓶内的压强值约为_____kpa。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com