
【题目】现有下列仪器或装置,请回答下列问题:
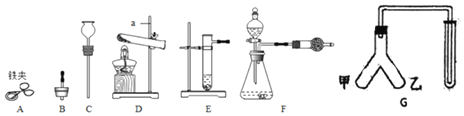
①仪器a的名称是______:用______![]() 填仪器名称
填仪器名称![]() 取废铁屑放入试管,可以用图A~E仪器组装成制取气体的发生装置:用废铁屑与稀盐酸反应制取H2,应选______
取废铁屑放入试管,可以用图A~E仪器组装成制取气体的发生装置:用废铁屑与稀盐酸反应制取H2,应选______![]() 填字母
填字母![]() ,写出反应的化学方程式:______。
,写出反应的化学方程式:______。
②选择气体收集方法时,必须考虑的气体性质有______![]() 填序号
填序号![]() 。
。
A 颜色 B 密度 C 溶解性 D 可燃性
③向“人”字型管G装置![]() 端分别装入一种固体和一种液体物质,按图示连接好装置,再倾斜装置,使乙中液体流入甲中。填写下表。
端分别装入一种固体和一种液体物质,按图示连接好装置,再倾斜装置,使乙中液体流入甲中。填写下表。
操作及现象 | 所装固体物质和液体物质 | 两端物质反应的化学方程式 |
将带火星木条放在试管口,木条复燃 | ______ | ______ |
将燃着木条放在试管口,木条熄灭 | ______ | ______ |
④若要检验F装置中产生的气体中是否含有水蒸气,干燥管中应该装入的物质是______。
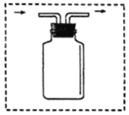
⑤若用如图装置且正放在桌上进行“排空气法”收集制取的H2,请把图中的“导气管”补画完整_____。
【答案】铁架台 药匙 ACE Fe+2HCl=FeCl2+H2↑ BC 二氧化锰和过氧化氢溶液 2H2O2![]() 2H2O+ O2↑ 大理石或石灰石和稀盐酸 CaCO3+2HCl=CaCl2+H2O+CO2↑ 白色的硫酸铜固体
2H2O+ O2↑ 大理石或石灰石和稀盐酸 CaCO3+2HCl=CaCl2+H2O+CO2↑ 白色的硫酸铜固体 
【解析】
①仪器a的名称是铁架台;药匙可以取粉末状药品;用废铁屑与稀盐酸反应制取H2,反应物是固体和液体,不需加热,发生装置应选ACE,铁和稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl=FeCl2+H2↑;
②选择气体收集方法时,必须考虑的气体性质有:密度和溶解性;故选BC;
③氧气具有助燃性,能使带火星的木条复燃,将带火星木条放在试管口,木条复燃,说明是氧气;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,所装固体物质和液体物质是二氧化锰和过氧化氢溶液,反应的化学方程式为:2H2O2![]() 2H2O+ O2↑;将燃着木条放在试管口,木条熄灭,说明是二氧化碳;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,所装固体物质和液体物质是大理石或石灰石和稀盐酸;大理石或石灰石主要成分是碳酸钙,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
2H2O+ O2↑;将燃着木条放在试管口,木条熄灭,说明是二氧化碳;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,所装固体物质和液体物质是大理石或石灰石和稀盐酸;大理石或石灰石主要成分是碳酸钙,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
④白色的硫酸铜固体遇与变蓝色。若要检验F装置中产生的气体中是否含有水蒸气,干燥管中应该装入的物质是:白色的硫酸铜固体;
⑤收集制取的H2要从短管进入,因为氢气的密度比空气小;
故答案为: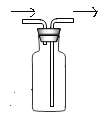 。
。


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:初中化学 来源: 题型:
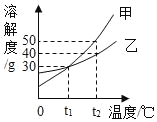
【题目】如图所示是甲、乙两种固体的溶解度曲线。若甲中含有少量乙,提纯甲的方法是_____;t2℃时,分别配制150g甲、乙的饱和溶液,所需要固体的质量关系为甲_____(选填“大于”、“小于”或“等于”)乙;t2℃时,将50g溶质质量分数为10%的甲溶液的质量分数变为20%,需要加入甲物质的质量是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图物质的溶解度曲线,判断下列说法正确的是

A. 将乙的饱和溶液过滤,能得到不饱和溶液
B. t1℃时,甲溶液、乙溶液的溶质质量相等
C. t2℃185g甲溶液降温至t1℃时,能析出49g晶体
D. 将26%的甲溶液从t2℃降温到t1℃时,溶质质量分数不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组的同学对铝的相关知识进行探究。
(知识回顾)
(1)铝是地壳中含量最多的金属元素,在自然界主要以化合态的形式存在于氧化铝中。下列说法不正确的是 _____。
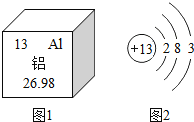
A 铝原子的中子数为13
B 铝离子核外有三个电子层
C 化合物中铝元素通常显+3价
D 铝可作导线是由于它具有良好的导电性
(铝的冶炼)
工业上常用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝,工艺流程如图。氧化铝是两性氧化物,与酸、碱都能发生反应,Al2O3+2NaOH=2NaAlO2+H2O。请回答以下问题:
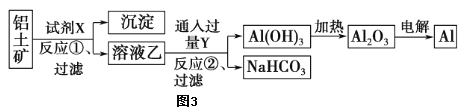
(2)试剂X是_________选填氢氧化钠溶液或盐酸)。
(3)反应①后过滤所得的沉淀是___________。
(4)写出反应②的化学方程式___________________。
(定性研究)
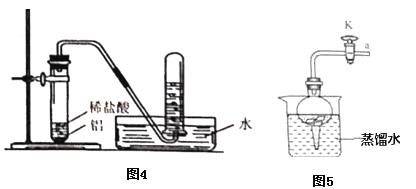
(提出问题)如图所示装置中铝和稀盐酸反应可以制取氢气,那么铝能否与水反应生成氢气呢?
(查阅资料)
物质 | 钠与水 | 铝与水 | 汞与水 |
能否发生反应 | 能反应 | 能反应 | 不反应 |
(交流与讨论)
(5)铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,起到保护膜的作用。如生活中可用铝壶烧水。铝与氧气反应的化学方程式为_____________。
(6)除去铝表面氧化铝薄膜的方法有(举一例)_______。除上述方法外,还可以将铝片浸入氯化汞( HgCl2)溶液中,形成铝汞齐(铝汞合金)破坏铝表面致密的氧化膜且防止其重新生成。
(实验探究)
(7)将铝片完全浸入氯化汞(HgCl2)溶液中1分钟左右,取出,立即用流水冲洗干净后加入到蒸馏水中(如图),其表面生成大量气泡、周围出现白色沉淀。若关闭导管上的活塞K,反应停止,其原理是_____________。
(8)在导管口a处涂肥皂水,发现导管口有气泡形成,当气泡离开导管后,气泡______(填“下沉”或“上升”),用燃着的木条点燃气泡,发出爆鸣声。
(实验结论)
(9)铝能与水反应生成氢气。写出铝与水反应生成氢氧化铝和氢气的化学方程式____________。
(定量研究)兴趣小组取8g铝镁合金样品,将30g氢氧化钠溶液平均分成三份依次加入样品中(镁与氢氧化钠溶液不反应,铝与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑),充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
剩余固体的质量/g | 5.3 | 2.6 | 2.0 |
(10)该合金中,镁与铝的质量比为 _____。
(11)所用氢氧化钠溶液中溶质的质量分数为多少?(写出计算过程)____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列反应属于置换反应类型的是![]()
![]()
A. CH4+2O2![]() CO2+2H2O
CO2+2H2O
B. Na2CO3+2HCl=2NaCl+H2O+CO2↑
C. Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
D. Zn+2AgNO3=2Ag+Zn(NO3 )2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(2分)【资料获悉】铁在高温条件下与氧化铜反应:2Fe+3CuO![]() Fe2O3+3Cu
Fe2O3+3Cu
铜在氯化铁溶液中发生反应:Cu+2FeCl3=2FeCl2+CuCl2
一定质量的铁与氧化铜的混合物,在高温条件下恰好完全反应.将反应后的固体粉末倒入盛有足量稀盐酸的烧杯中,振荡,充分反应后静置,然后从烧杯中取适量溶液(表示为“甲”)于试管中,并加入一定质量的锌粉,充分反应后过滤,得到滤液乙和固体丙.下列判断正确的是( )
①甲中不含FeCl3;
②甲中含有FeCl3;
③若向固体丙加稀盐酸无明显现象,则滤液乙中一定含有ZnCl2、FeCl2,可能含有CuCl2;
④若向固体丙加稀盐酸有气体产生,则滤液乙中可能含有ZnCl2、FeCl2,一定不含有CuCl2.
A.①③ B.②③ C.①④ D.②④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家已经在实验室中制造出了冰7.这种冰需要在含有大量水源和极高的压强下才能够生成,水分子会整齐排列成排或排成一列非常整齐有规律的冰晶,像是一个立方体的牢笼聚合物。下列说法不正确的是( )

A. 冰7中分子之间的距离比普通冰中的小
B. 海水在一定条件下可以形成冰7
C. 冰7中的分子永不停息地运动
D. 冰7和水的化学性质不完全相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是
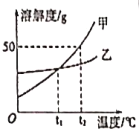
A. t1℃时,甲、乙两种物质的溶液中溶质的质量分数相等
B. 由t2℃降温到t1℃,甲饱和溶液比乙饱和溶液析出晶体的质量多
C. t2℃时,将40g甲物质加入50g水中.充分溶解后溶液的质量为90g
D. 甲物质中含有少量的乙杂质,要提纯甲物质可以采用降温结晶
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线。

下列说法正确的是
A. 在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V时所得溶液的pH越大
B. 在a曲线所示的实验中,若用酚酞做指示剂,酚酞溶液由红色变为无色
C. 在a、b、c三种曲线所示的实验中,反应速率相同
D. 在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com