
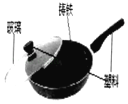
【题目】铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图。
(1)所标物质中,属于合金的是_____;含有的金属单质是_____。
(2)炒菜时铁锅中的油着火可用锅盖盖灭,其原理是_____。
(3)铝锅轻便、耐用,其原因是_____、_____。
(4)为比较铝和铁的金属活动性,某同学设计实验方案:将铝和铁分别放入盐酸中,比较反应的剧烈程度,你认为该方案_____(填“合理”或“不合理”),理由是_____。
(5)废旧铁锅、铝锅不要随意丢弃,应回收利用,这样做的意义是_____。
【答案】铸铁; 铁 使油与氧气隔绝; 铝的密度小; 常温下,与氧气反应表面生成致密的氧化铝薄膜,阻止铝的进一步氧化; 不合理; 只有相同条件下才有可比性(如铝表面致密的氧化物薄膜、金属的质量和表面积不相等等条件不同时,不能证明结论); 减少环境污染,节约金属资源。
【解析】
(1)铸铁属于生铁,是合金;含有的金属单质是铁;
(2)油着火可用锅盖盖灭,利用的是隔绝氧气的灭火原理。
(3)铝的密度小,所以铝锅轻便;常温下,以与氧气反应表面生成致密的氧化铝薄膜,阻止铝的进一步氧化,因此铝锅比较耐用。
(4)铝和铁与稀盐酸接触面积若不同,是不能进行比较,只有相同条件下才有可比性,所以这种方法不能得出谁的活动性更强;
(5)回收利用废旧铁锅、铝锅,可以减少环境污染,而且还可以节约冶炼金属时所用到的大量的煤等化石燃料和铁矿石等矿石资源。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:初中化学 来源: 题型:
【题目】对于下列几种化学符号,有关说法正确的是
①H ②Fe2+ ③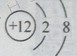 ④P2O5 ⑤ KClO3
④P2O5 ⑤ KClO3
A.表示物质组成的化学式有①④⑤
B.④中数字“5”表示五氧化二磷中有5个氧原子
C.表示阳离子的有②③
D.⑤中氯元素的化合价为-1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是目前世界年产量最高的金属。请回答。
(1)生活中,用铁锅炒菜是利用了金属铁的_______性。
(2)验证铁和铜的金属活动性顺序,除铁外还需要用到的一种试剂是_________。
(3)小倩同学根据工业炼铁的原理设计了如下图所示装置进行实验。
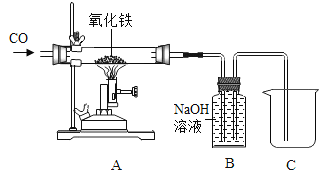
①实验开始时,应先给氧化铁加热还是通一氧化碳______?
②加热一段时间后,A装置玻璃管内的现象是______,反应的化学方程式为_____________。
③你认为该装置是否需要添加尾气处理装置并说明理由 _______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是研究物质的,而物质是由肉眼看不见的微观粒子构成的,让我们从五彩缤纷的宏观世界步入神奇的微观世界。如图是两种溶液恰好完全反应的微观示意图。
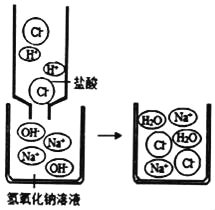
(1)请写出此反应的化学方程式______。
(2)该反应是酸和碱的______反应,又属于______反应(基本反应类型)
(3)反应前后不变的微粒有______(填离子符号)。
(4)从微观的角度分析该反应能发生的实质是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝土矿中含40%~60%Al2O3,1%~15%SiO2、7%~30%Fe2O3,从铝土矿中提取氧化铝的过程如图:
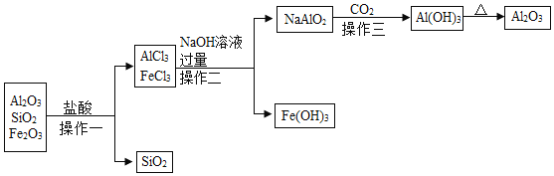
(已知:SiO2不溶于水,NaAlO2溶于水,Al(OH)3+NaOH=NaAlO2+2H2O,2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3)
(1)操作一、操作二、操作三三个步骤中都要采用的分离方法是______;
(2)写出操作一发生反应的化学方程式______;
(3)从铝土矿中提取Al2O3时,经历了“Al2O3-AlCl3-NaAlO2-Al(OH)3-Al2O3”的转化过程,请分析这样做的目的是什么?______;
(4)操作二中NaOH溶液过量的目的是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组为了探究影响过氧化氢分解快慢的因素,进行了下列实验:
实验 序号 | 过氧化氢溶液浓度 | 过氧化氢溶液的体积/mL | 温度/℃ | 二氧化锰的用量/g | 收集氧气的体积/mL | 收集氧气所需的时间/s |
1 | 5 | 1 | 20 | 0.1 | 4 | a |
2 | 15 | 1 | 20 | 0.1 | 4 | b |
3 | 30 | 5 | 35 | 0.1 | 4 | c |
4 | 30 | 5 | 55 | 0.1 | 4 | d |
(1)欲探究温度在实验中是否有影响,应该比较_____(填实验序号):从实验收集的是数据看,a>b,即实验②收集等量氧气所需时间比实验①少,由此可得出的结论是_____。
(2)请写出过氧化氢分解的化学方程式:_____。
(3)除测定收集相同体积的氧气所需的时间外,还可通过测定_____的方法比较过氧化氢分解的快慢。
(4)若其他条件相同,则催化剂的种类可能会影响到催化效果请设计实验方案进行验证:_____。
(5)该小组同学还使用了压强传感器测不同质量的二氧化锰对过氧化氢分解反应的影响,他在8mL 3%的过氧化氢溶液中分别加0.03g、0.06g、0.08g、0.12g、0.24g的二氧化锰,压强的变化曲线如图所示(说明,曲线的斜率表征催化剂反应的速率)。
请相据图示写出两条规律性的结论:
(1)_____,(2)_____。
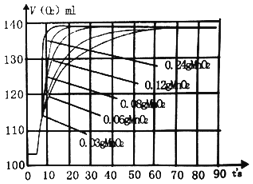
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在锥形瓶中加入10g 久置且表面氧化的锌粒(锌粒中原杂质不与稀硫酸反应),再滴加稀硫酸(H2SO4),放出气体的质量与所加稀硫酸(H2SO4)质量的关系如图所示,请回答下列问题:
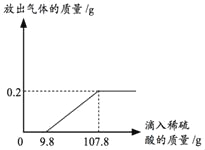
(1)产生氢气_____g;该锌粒中单质锌的质量分数是_____;
(2)刚开始滴加稀硫酸没有氢气(H2)产生,其原因是_____。
(3)求所滴加的稀硫酸(H2SO4)中溶质的质量分数是多少?_____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。请回答下列问题:
(1)煤是复杂的混合物,主要含______元素。
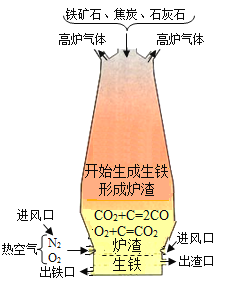
(2)煤的加工产品有很多用途,其中焦炭广泛应用于炼铁。如图是高炉炼铁的示意图。请根据图例回答:
①焦炭在炼铁过程中的主要作用是:______;
②请用化学方程式表示炼铁的原理:______;
③高炉炼铁过程中会产生大量的高炉气体,其主要成分是高浓度的CO和氧化铁尘粒。请你对高炉气体的处理提出合理化的建议:______
(3)化肥厂合成并生产氨的原料是煤、空气、水。其生产简要流程如图:
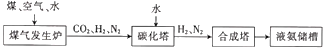
煤气发生炉中发生的主要反应有①C+O2![]() CO2;②C+H2O
CO2;②C+H2O![]() CO+H2.两个反应必须进行调控才能保持一定的炉温。其中反应②会______(填“放出”或“吸收”)热量。将合成的氨气部分通入碳化塔,既除去了二氧化碳又得到了化肥NH4HCO3,试写出该反应的化学方程式:______。
CO+H2.两个反应必须进行调控才能保持一定的炉温。其中反应②会______(填“放出”或“吸收”)热量。将合成的氨气部分通入碳化塔,既除去了二氧化碳又得到了化肥NH4HCO3,试写出该反应的化学方程式:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)实验室部分仪器或装置如图所示。请回答下列问题。
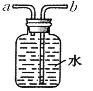

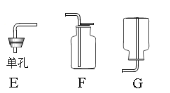
(1)若用高锰酸钾制取氧气,你认为还需增加的仪器是 ,实验时该装置试管口应放一团棉花,其目的是 ;用高锰酸钾制取氧气的化学方程式为 。用下图所示装置收集氧气,氧气应从____(填“a”或“b”)端导入。
(2)若要组装一套二氧化碳的发生和收集装置,可选择上图中的_______(填标号)。 实验室制取二氧化碳的化学方程式为 。
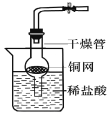
(3)某同学借助干燥管、烧杯、铜网等仪器装配了一个在实验室中制取二氧化碳气体的装置,如图所示。在干燥管内的铜网上应盛放 ;若将铜网换成铁网,会产生什么后果? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com