
| A. | 过氧化氢溶液的浓度相同 | |
| B. | 催化剂的质量一定相同 | |
| C. | 反应前过氧化氢溶液的温度一定相同 | |
| D. | 反应容器的体积一定相同 |
分析 对应实验影响因素的探究,要注意变量的控制,注意要让除探究要素(本题就是研究不同的催化剂的影响)所以除催化剂种类不同之外,其他都应该是相同的.
解答 解:对于反应速率的影响,可能影响到反应速率的因素:
1、反应物的角度:反应物的状态(固体或者液体等,当同样都是固体时,要大小和形状都相同)和质量分数.是指全部反应物.
2、反应的条件:指温度或者类似搅拌等,要让温度相同.当反应需要加热进行时,要让反应装置时要用相同的受热仪器,以便温度能够达到相同.
3、催化剂.采用的催化剂的种类和质量还有催化剂的状态都影响.
所以在控制变量时要注意以上细节.
A、过氧化氢溶液中溶质的质量分数一定相同是反应物的要素.
B、催化剂的质量一定相同是对催化剂的控制,其实更严谨的说法是催化剂的质量相同的同时也要注意催化剂的状态也要相同,比如都是粉末,粉末颗粒要相同.
C、反应前过氧化氢溶液的温度一定相同是反应物的要素.
D、由于本实验是在常温下进行的,所以对加热就没有要求,所以装置可以是不同的.
故选:D.
点评 实验变量的控制要注意对要素考虑的周全,针对不同的要素进行严格控制,从而让结果更有说服力.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:填空题
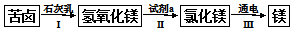

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
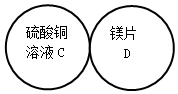 用四个圆表示A(铁片)、B(稀硫酸)、C(硫酸铜溶液)、D(镁片)四种物质,用两圆相切表示两种物质可以发生反应,如图所示.请回答下列问题:(提示:物质间均恰好完全反应,其中稀硫酸与硫酸铜溶液不反应)
用四个圆表示A(铁片)、B(稀硫酸)、C(硫酸铜溶液)、D(镁片)四种物质,用两圆相切表示两种物质可以发生反应,如图所示.请回答下列问题:(提示:物质间均恰好完全反应,其中稀硫酸与硫酸铜溶液不反应)查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 装有过氧化氢溶液的试管中伸入带火星的木条 | 木条不复燃 | 常温下过氧化氢溶液的分解速率很慢 |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,将带火星的木条伸入试管中 | 木条复燃 | Al2O3能加快过氧化氢的分解速率 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图所示是测定空气中氧气含量的装置图.
如图所示是测定空气中氧气含量的装置图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的纯碱溶液,请在图中画出溶液的pH随滴入纯碱的量的大概变化图象,并解释各段变化的理由.
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的纯碱溶液,请在图中画出溶液的pH随滴入纯碱的量的大概变化图象,并解释各段变化的理由.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
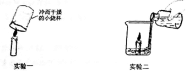 如图是有关蜡烛燃烧的两个实验,请回答有关问题.
如图是有关蜡烛燃烧的两个实验,请回答有关问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com